GIPが過食・肥満・糖尿病を改善することを解明 「GIP/GLP-1受容体作動薬」治療に根拠 新規インクレチン治療の確立へ
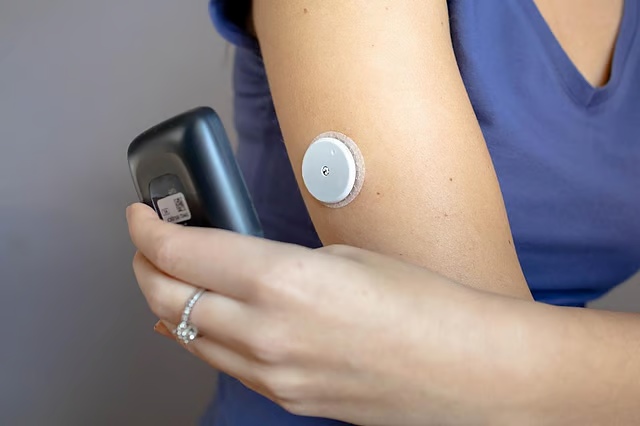
GIP受容体作動薬が"痩せホルモン"のレプチンの分泌を誘導することを解明
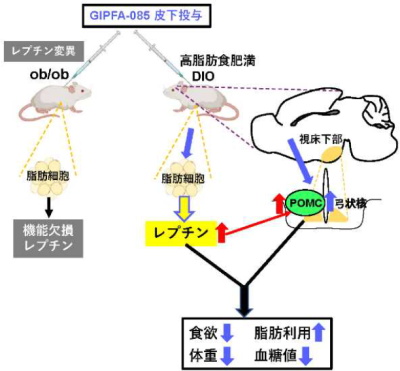
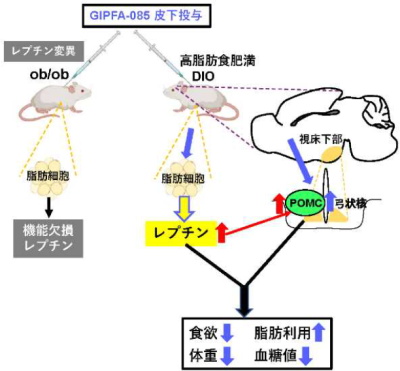
IPFA-085によるレプチン分泌とPOMC神経活性化を
介した食欲・体重・血糖値低下(抗肥満・糖尿病作用)
食事にともない消化管から分泌され、膵に作用してグルコース誘発インスリン分泌を促進するインクレチンには、「グルカゴン様ペプチド1(GLP-1)」と「グルコース依存性インスリン分泌刺激ポリペプチド(GIP)」がある。
インクレチンの代表的なものとしてGLP-1とGIPがあるが、これらは生体の分解酵素で速やかに切断されるため、分解酵素耐性の分子修飾をした長時間作用型の受容体活性化分子(受容体作動薬)が作られている。
長時間作用型のGLP-1受容体作動薬は、すでに糖尿病治療薬として使用されており、血糖降下に加えて体重・摂食低下の作用を示すことから、米国では肥満への適応が承認されている。
一方、GIPは、肥満との関連が指摘されてきたにも関わらず、GIP受容体作動薬は単独およびGLP-1受容体作動薬との併用で体重・摂食低下を示すため、"GLP-1パラドックス"として注目されている。
その解決には、GIPの体重、摂食への作用の解明が不可欠となる。そこで岐阜大学などの研究グループは、特異的なGIP受容体作動薬であるGIPFA-085の作用を調べた。
高脂肪食負荷肥満(DIO)マウスで、GIPFA-085の皮下投与により、満腹誘導・代謝亢進作用を有する脂肪ホルモン「レプチン」分泌を誘導し、摂食量低下と脂肪利用増加を起こし、1日1回連日投与することで、体重および血糖値を12日目まで低下させることを確かめた。
脂肪細胞から分泌されたレプチンは、摂食を抑制し、エネルギー消費を亢進し、体重を低下させる。アディポカインのなかで、レプチンは最初に発見され、もっとも重要なもののひとつとみられている。
一方、機能的レプチン欠損ob/obマウスではGIPFA085は効果がなかった。
GIPFA-085は、摂食・代謝の司令塔である視床下部弓状核・POMC神経を直接活性化し、その際レプチンと協働作用を発揮したとしている。
POMC神経の活性化は、強力な摂食抑制を起こし、また交感神経を介して末梢に情報を送り、エネルギー消費亢進・体重低下・血糖値低下を起こす。レプチンはこの神経を標的として、中枢性の摂食・体重・血糖低下作用を発揮すると考えられている。
GIP/GLP-1二重受容体作動薬の治療の根拠を与える発見
研究は、関西電力医学研究所統合生理学研究センターおよび岐阜大学医学系研究科糖尿病・内分泌代謝内科学/膠原病・免疫内科学の矢田俊彦センター長・客員教授、韓婉昕医学研究員、矢部大介教授、関西電力医学研究所の清野裕研究所長、京都府立大学大学院生命環境科学研究科 応用生命科学専攻 岩﨑有作教授らの研究グループによるもの。研究成果は、「Diabetes Obesity And Metabolism」にオンライン掲載された。
「本研究結果によって、GIP受容体作動薬であるGIPFA-085はレプチン分泌を引き起こし、レプチンとの協働作用により弓状核POMC神経を活性化させ、摂食抑制と体重低下を起こし、血糖を制御して、過食・肥満・糖尿病を改善することを明らかにした」と、研究グループでは述べている。
研究グループは研究の意義として、(1) GIPの食欲抑制、肥満改善作用を明らかにし、(2) GIP受容体作動薬による新規インクレチン治療を確立し、(3) 近く肥満を適応として承認が予想されるGIP/GLP-1二重受容体作動薬の治療の根拠を与えることを挙げている。
今後の展開としては、次のことを挙げている。
▼ GIP受容体作動薬(GIPFA-085)によるレプチン分泌促進の機序の解明:脂肪細胞のGIP-1受容体活性化によるレプチン合成および分泌の検証。
▼ GIP受容体作動薬による脂肪利用亢進(脂肪分解促進)の機序の解明。レプチンの脂肪細胞への直接効果、および、交感神経活性化を介した脂肪細胞への効果の関与の解析。
▼ GIP受容体作動薬とGLP-1受容体作動薬の併用による強力な摂食・体重・血糖値低下の機序の解明:協働作用発揮におけるレプチンの役割の検証。
▼ 病態成因と程度が異なる糖尿病・肥満モデルマウスを用いて、レプチン機能(分泌、作用など)の質的・量的変化とGIP受容体作動薬の有効性の関係を調べる。その結果から、GIP受容体作動薬またはGIP/GLP-1二重受容体作動薬により代謝改善が期待される糖尿病・肥満者の予測、選択につながると期待される。
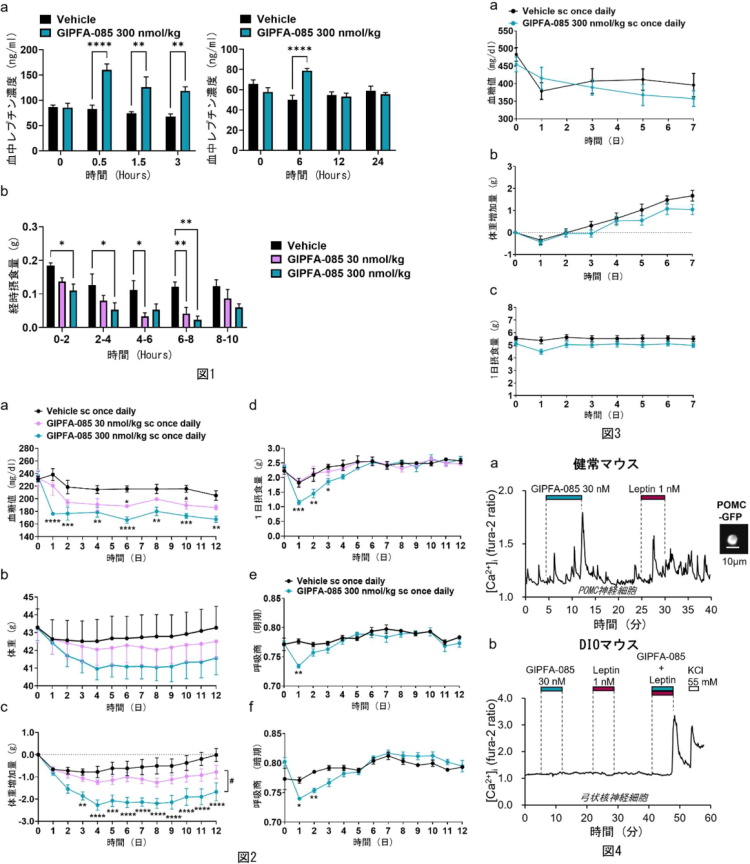
高脂肪食負荷肥満(DIO)マウスに、GIPFA-085を皮下投与すると、投与1時間後から糖負荷試験での血糖値と摂食量を低下させ、血中レプチン濃度を増加させた(図1a)。
GIPFA-085(300nm/kg)を連日投与すると、投与後1~3日目で摂食量が低下し(図2d)、呼吸商が低下(脂肪利用亢進)し(図2e、f)、1~12日目で血糖値が低下(図2a)、3~12日目で体重が低下(4%)し(図2b、c)、投与中止後リバウンドはみられなかった。
関西電力医学研究所
岐阜大学医学系研究科糖尿病・内分泌代謝内科学/膠原病・免疫内科学
Glucose-dependent insulinotropic polypeptide counteracts diet-induced obesity along with reduced feeding, elevated plasma leptin and activation of leptin-responsive and proopiomelanocortin neurons in the arcuate nucleus (Diabetes Obesity and Metabolism 2023年2月28日)