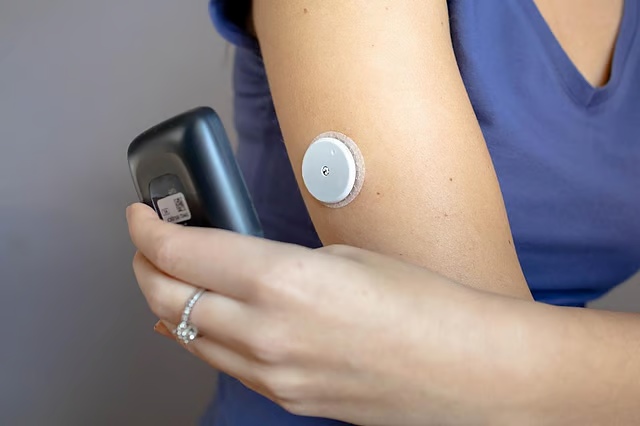
GIP/GLP-1受容体作動薬チルゼパチドが肥満2型糖尿病患者の体重を平均16%減少
発表されたデータは、チルゼパチドの有効性と安全性を検討した国際共同プラセボ対照無作為化二重盲検試験である「SURMOUNT-2」の結果。研究参加国には日本も含まれている。938人の過体重・肥満を伴う2型糖尿病患者をチルゼパチド10mg群、同15mg群、プラセボ群に1対1対1で割り付け72週間介入した。チルゼパチドが割り当てられた患者では、週1回2.5mgから開始し、4週ごとに2.5mgずつ増量された。
介入による体重変化率を見ると、まず、治験薬の投与が中止されていた場合にはその中止前のデータを用いた解析で、プラセボ群では-3.3%であったのに対して、チルゼパチド10mg群は-13.4%、同15mg群は-15.7%であった。5%以上の体重減少を達成した割合は、同順に30.5%、81.6%、86.4%だった。
次に、投与中止を考慮せずに解析した結果を見ると、プラセボ群が-3.2%、チルゼパチド10mg群は-12.8%、同15mg群は-14.7%の減量幅であり、5%以上の体重減少を達成した割合は、32.5%、79.2%、82.7%だった。
最も多く認められた有害事象は消化器症状であり、嘔気が10mg群で20.2%、15mg群は21.9%、下痢は同順に19.9%、21.5%、嘔吐10.9%、13.2%、便秘8.0%、9.0%などと報告されている。有害事象による投与中止率は10mg群3.8%、15mg群7.4%、プラセボ群3.8%、全ての理由による中止率は同順に9.3%、13.8%、14.9%だった。
この発表に基づき米CNNは、「チルゼパチドは、米国において既に血糖降下薬としてはオゼンピック、肥満改善薬としてはWegovyという名称で販売されているセマグルチドの、強力なライバルとなる可能性がある」と報じている。チルゼパチドの減量効果に関しては昨夏、「The New England Journal of Medicine」に、非糖尿病肥満者で最大22%の減量が達成されたとの研究結果が報告されている。その時の研究と今回の研究の結果は、同薬の体重管理薬としての迅速承認を米食品医薬品局(FDA)へ求めるイーライリリー社からの申請データに用いられる予定。
なお、同効薬であるノボノルディスク社のセマグルチドはFDAにより、肥満関連合併症がある場合の減量目的での使用が承認されている。そのセマグルチドに関しては治験時に、非糖尿病肥満者の体重を12.4%低下させることが示されていた。イーライリリー社は現在、米国とカナダの非糖尿病肥満者700人を対象として、チルゼパチドとセマグルチドの有効性と安全性を比較する研究を計画している。
[HealthDay News 2023年4月27日]
Copyright ©2023 HealthDay. All rights reserved.
Photo Credit: Adobe Stock