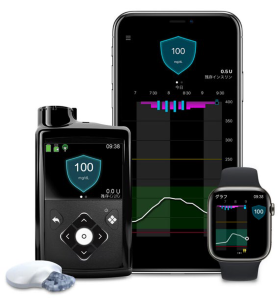
【新型コロナ】オミクロンを含むすべての変異株に対して中和活性が高い「ナノボディ抗体」を創出
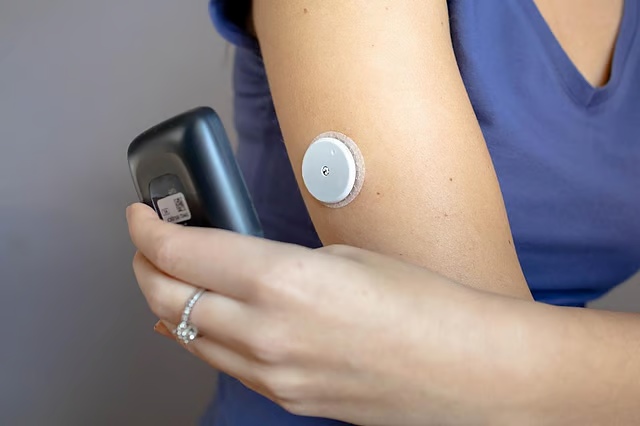
新型コロナウイルスを中和する抗体 オミクロンを含む全ての変異株に有効
京都大学や大阪大学などの研究グループは、新型コロナウイルスの「懸念される変異株(VOC)」である「オミクロン株(B.1.1.529, BA系統)」を含むすべての変異株に対して、これまで使用されてきたどの治療用抗体製剤よりも中和活性が高い「ナノボディ抗体」を創出したと発表した。
ナノボディ抗体は、VHH抗体とも呼ばれており、アルパカなどのラクダ科の動物とサメ科の動物がもつ重鎖のみからなる特殊な抗体。ヒトや他の動物の抗体は、重鎖と軽鎖からなるより複雑で大きな分子となっている。
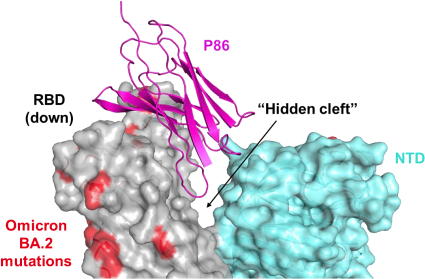
さらに、生体分子を極低温下で観察し構造を解析できるクライオ電子顕微鏡を用いた立体構造解析から、これらのナノボディ抗体は新型コロナウイルス表面にあるスパイクタンパク質の深い溝をエピトープにしていることが示された。
エピトープは、抗体が結合する生体分子のある特定の部位で、エピトープが変異したウイルスは、抗体による免疫系を逃れることができる。
発見したエピトープは、ヒトの抗体が到達できない部分であり、新型コロナウイルスのほぼすべての変異株で、変異のみられない共通の構造をしているという。
新型コロナウイルスは、変異を繰り返して広まり、現在主流である「オミクロン株」は、それまでのVOC(アルファ株、ベータ株、ガンマ株、デルタ株)に比べ、スパイクタンパクの変異箇所が圧倒的に多く、以前感染した人やワクチン接種者にも感染する。また、オミクロン株による新型コロナには、その出現前に開発された治療用抗体のほとんどが効かなくなることが明らかになっている。
ワクチンで誘導される中和抗体や、これまでに開発された治療用抗体は、新型コロナウイルス上のスパイクタンパク質の表面に結合して、感染を抑えるものが多い。
研究で創られたナノボディ抗体は、ヒト抗体の10分の1の大きさで、小型の抗体であれば、スパイクタンパク質の表面よりも奥まった深い溝(研究グループはクレバスまたは隠された裂け目と呼んでいる)に結合できる。
ナノボディ抗体は新型コロナウイルスへの結合力がきわめて強く、環境安定性も高いため、下水などの環境中のウイルスを濃縮し、検出する用途にも応用することもできる。
スパイクタンパク質にナノボディ抗体が結合した構造
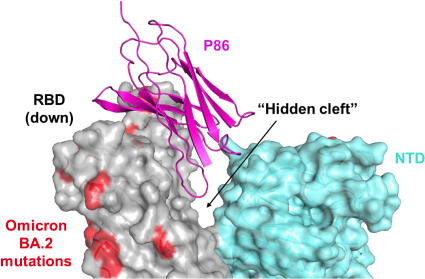
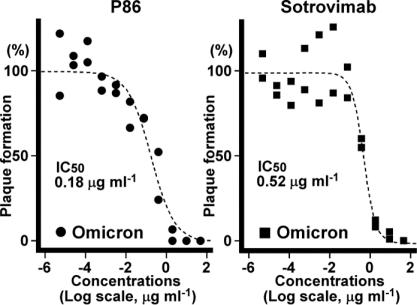
ナノボディ抗体(P86)のオミクロン株(BA.1)への中和活性
研究は、京都大学大学院医学研究科の高折晃史教授、大阪大学大学院生命機能研究科の難波啓一特任教授、藤田純三特任助教(常勤)、COGNANO(コグナノ)らの研究グループが、大阪大学感染症総合教育研究拠点/微生物病研究所、横浜市立大学、東京大学の研究グループとの共同で行ったもの。研究成果は、英科学誌「Communications Biology」にオンライン掲載された。
ナノボディ抗体は遺伝子工学による改変がしやすく、ヒト抗体よりも数千倍安価に生産できる。高折教授らは、研究で得られた知見にもとづき、より中和活性の高い改変ナノボディ抗体を作成し、臨床応用を目指すとしている。
京都大学、大阪大学、COGNANOでは現在、さまざまな感染症について、ウイルス学的な解析や、中和抗体やナノボディ抗体の構造解析についての研究に取り組んでおり、新型コロナウイルスのみならず、エイズウイルス(HIV)、ネコエイズウイルス、サル痘、その他、がん免疫を明らかにするための研究を推進している。
「ナノボディ技術を使用することで、従来のヒト抗体ではなしえなかった広い中和活性をもつ抗体を開発し、そのエピトープを同定した。今後、新たなCOVID-19治療薬の開発につなげると同時に、本技術を新たな感染症治療に対応可能なパイプラインにしたい」と、高折教授は述べている。
京都大学大学院医学研究科
大阪大学大学院生命機能研究科
COGNANO
A panel of nanobodies recognizing conserved hidden clefts of all SARS-CoV-2 spike variants including Omicron (Communications Biology 2022年7月6日)