肥満をたらす食欲を制御するタンパク質を発見 脳内で食欲や代謝を制御 欠損するとレプチンとインスリンの両方が効かない抵抗性に
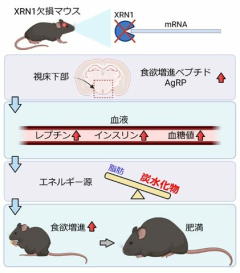
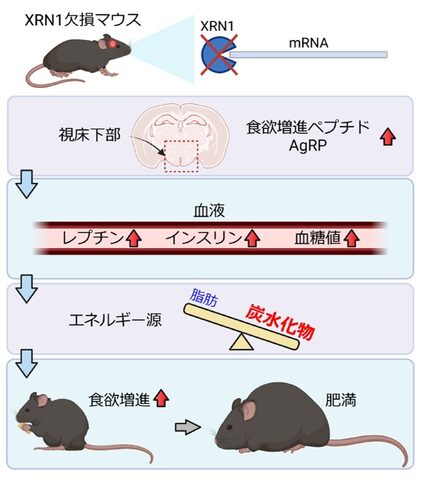
脳内で食欲や代謝を制御するのに重要な役割を果たしているXRN1
研究は、沖縄科学技術大学院大学細胞シグナルユニットの山本雅教授、栁谷朗子氏、髙岡翔平博士氏、モハメッド ハイサム氏らの研究グループによるもの。研究成果は、米科学誌「iScience」に掲載された。
肥満は循環器病や2型糖尿病、がんなど多くの疾患と関係している。肥満は基本的に食事摂取量とエネルギー消費量の不均衡により起こるが、脳がどのように膵臓や肝臓、脂肪組織などの末梢組織と協調して、食欲や代謝を制御しているかについては明らかになっていない。
そこで研究グループは、メッセンジャーRNA(mRNA)分解の最終段階を制御し、遺伝子活性に重要な役割をしている「XRN1」というタンパク質に着目した。
研究グループは、脳(前脳)の一部でXRN1を欠損したマウスを作製して実験した。その結果、脳内にXRN1がないマウスは生後6週間で急速に体重が増え始め、生後12週までに肥満になった。マウスの体内の脂肪組織や肝臓などに脂肪が蓄積していることを確認できた。また、欠損マウスは、対照群の正常マウスと比べて1日当たりの摂食量が約2倍に増えていた。
XRN1欠損マウスの過食の原因を調べるために、食欲を抑えるレプチンの血中濃度を測定した。すると、欠損マウスは正常マウスと比べて有意に高い値となっていた。レプチン量が正常であればマウスは食欲を感じなくなるはずで、欠損マウスはレプチンの濃度が高くなってもその効果があらわれず、食欲が抑制されないという「レプチン抵抗性」があることが判明した。
さらに、XRN1欠損マウスは加齢にともない、インスリンの値がレプチン値の上昇とともに著しく高くなることも確認した。欠損マウスはレプチンに反応しなかったために摂食行動を続けて血糖値が上がり、その結果インスリン値も上がったとみられる。
研究グループはさらに、エネルギー消費量の低下も肥満の原因であるかどうかを調べるため、マウスを酸素消費量が測定できる特殊なケージに入れて間接的に代謝量を算出した。
その結果、6週齢のマウスは正常マウス、欠損マウスともエネルギー消費量に差はなかったが、正常マウスはもっとも活動的になる夜間に炭水化物を燃焼し、活動量の少ない日中に脂肪を燃焼するという切り替えができていたのに対し、欠損マウスは昼夜問わず脂肪を効率的に消費できず、炭水化物を主なエネルギー源としていたことが分かった。
XRN1欠損マウスは12週齢になると、対照マウスに比べてエネルギー消費量が減少した。これは肥満の原因ではなく、肥満によってマウスの活動性が低下したことによる結果であると考えられるという。
「XRN1がないと脂肪を効果的にエネルギー源として利用できないと考えられす。XRN1欠損により肥満になった原因は、レプチン抵抗性による過食だったと考えられます」と、研究グループでは述べている。
遺伝子が活性化すると、DNAからmRNAが作られ、そのmRNAから特定のタンパク質が作られる。細胞はさまざまな方法で遺伝子活性を調節するが、そのひとつにmRNAの分解速度を増減させる方法があり、それによってタンパク質の合成量を増減させる。
XRN1は、mRNA分解の最終段階を制御し、遺伝子活性に重要な役割を果たしている。肥満マウスの視床下部では、もっとも強力な食欲増進物質のひとつであるアグーチ関連ペプチド(AgRP)というタンパク質を作るmRNAが増加しており、そのためにアグーチ関連タンパク質の量が増加していることを明らかにした。
「レプチンは通常、アグーチ関連ペプチド産生神経(AgRPニューロン)の活動を抑制しますが、XRN1の欠損によりこのニューロンの活性が非常に高く維持され、レプチンのシグナルが無効化されている可能性があります」と、研究グループでは述べている。
「今後は、神経科学の研究ユニットと協力して、XRN1がどのように視床下部のニューロンの活動に影響を与えて食欲を調節するかを正確に解明したいと考えています」としている。
沖縄科学技術大学院大学細胞シグナルユニット
Neuronal XRN1 is required for maintenance of whole-body metabolic homeostasis(iScience 2021年10月22日)











