糖尿病治療のための膵島移植 移植後の副作用が少ない免疫抑制剤を開発 耐糖能障害を起こさず新生血管も阻害しない
東北大学は、この問題を解決するため、従来の免疫抑制剤とは異なる作用機序をもつ新規免疫抑制剤に着目し、その有効性や安全性を実証した。この新規免疫抑制剤は耐糖能障害を引き起こさないので、膵島移植のみならず膵臓移植にも有用であり、また移植細胞への新生血管も阻害しないので、肝細胞移植などのさまざまな細胞移植への応用を期待できるとしている。
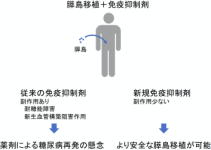
従来の免疫抑制剤と異なる作用機序 より安全な膵島移植を可能に
糖尿病の先端治療として、インスリンを分泌する膵島を患者に移植する治療法がある。しかし、現在の標準的免疫抑制剤には副作用があり、解決すべき喫緊の課題となっている。
そこで東北大学は、糖尿病治療のための膵島移植に最適な副作用が少ない免疫抑制剤(KRP-203)を見出すことに成功した。生体膜を構成するスフィンゴ脂質の代謝産物であるスフィンゴシン-1-リン酸の機能的アンタゴニストであるKRP-203は、冬虫夏草の培養液中から発見された化合物を化学修飾することで見出された。機能的アンタゴニストは、生体内の受容体分子に働いて神経伝達物質やホルモンなどの働きを阻害する薬剤だ。
KRP-203は、従来のカルシニューリン阻害剤とはまったく異なる作用機序を有しており、リンパ球の動きを封じ込めることで免疫調節機能を発揮する。課題となっていた耐糖能障害や移植膵島への新生血管阻害といった副作用を引き起こさないため、より安全な膵島移植が可能になるとしている。
研究は、東北大学大学院医学系研究科移植再生医学分野の後藤昌史教授、Ibrahim Fathi氏らの研究グループによるもの。研究成果は、米学術誌「Transplantation」に掲載された。
「この免疫抑制剤(KRP-203)は、従来の免疫抑制剤とはまったく異なる作用機序を有しており、研究成果は今後、膵島移植による糖尿病治療に大いに役立つと考えられます。さらに今後、肝不全に対する肝細胞移植など、他のさまざまな細胞移植治療への応用も期待されます」と、研究グループは述べている。
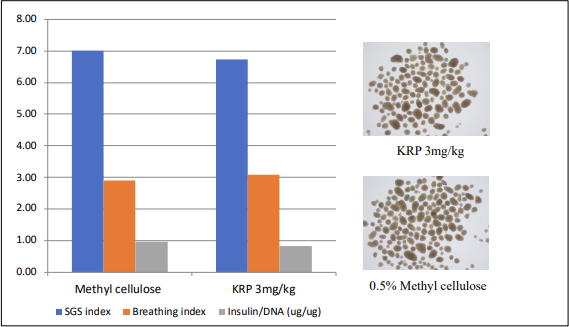
SGS index:In vitroの糖負荷試験で、高グルコース溶液で膵島が放出したインスリン量と低グルコース溶液で放出したインスリン量の比率(高い方が膵内分泌機能が良好であることを示す)
Breathing index:In vitroの糖負荷呼吸活性試験で、高グルコース溶液で計測された膵島の呼吸活性量と低グルコース溶液で計測された膵島の呼吸活性量の比率(高い方が膵内分泌機能が良好であることを示す)
Insulin/DNA:膵島のインスリン量と DNA 量の比率(高い方が膵内分泌機能が良好であることを示す)
KRP-203とシロリムスの併用でより効果的に免疫拒絶反応を制御
膵島移植は、脳死ドナーから提供された膵臓から膵島細胞のみを抽出し、糖尿病患者へ移植する治療法。全身麻酔や開腹手術を必要とせず、点滴の要領で短時間に終えることが可能だ。そのため、従来行われてきた膵臓移植などの臓器移植療法と比べ、安全・簡便・低侵襲などの利点が着目され、次世代の中心的移植医療になると期待されている。
一方で、他のすべての臓器移植と同様に、免疫拒絶反応を制御するために生涯にわたる免疫抑制剤の服用が必須となることが課題のひとつになっている。現在の標準的免疫抑制剤であるカルシニューリン阻害剤は、神経伝達を調整する作用をもつカルシニューリンを阻害することで、細胞内情報伝達作用を制御し、免疫担当細胞の活動を抑制することを目的とした薬剤だが、移植された膵島細胞に対して、耐糖能障害や新生血管構築阻害作用を示すことが広く知られている。
スフィンゴシン-1-リン酸の機能的アンタゴニストであるKRP-203は、リンパ球の動きを封じ込めることで免疫調節機能を発揮する。研究グループは、膵島機能と血管新生能に対するKRP-203の効果を糖尿病動物モデルで検証し、膵島移植におけるカルシニューリン阻害剤を含有しない新規免疫抑制プロトコールの樹立を試みた。
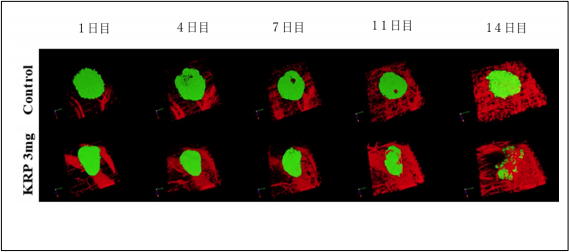
その結果、血糖値計測、糖負荷試験、分離膵島の機能評価で、KRP-203は耐糖能障害を惹起しないことが判明した。また、多光子レーザー走査型顕微鏡の解析で、KRP-203は膵島の新生血管構築作用も阻害しないことが明らかとなった。
さらにKRP-203は、同種の異なる個体間における移植の組み合わせである同種異系のモデルでの免疫拒絶反応を単剤でも効果的に制御することが可能で(44%)、シロリムスとの併用で相乗作用を発揮し、より効果的に免疫拒絶反応を制御できることが判明した(83%)。
今回の研究は、KRP-203と低用量シロリムスの併用が、膵島移植でのカルシニューリン阻害剤を含有しない新規免疫抑制プロトコールとして有望である可能性をはじめて示唆したもので、学術的な面からも臨床的な面からも高い意義を有するとしている。
研究は、杏林製薬によるKRP-203提供の協力のもと、文科省科学研究費挑戦的研究(萌芽)、科学技術振興機構地域産学官共同研究拠点整備事業(TAMRIC)、および東北大学大学院医学系研究科共通機器室によって支援された。
 移植膵島および膵島周囲の新生血管の経時的変化
移植膵島および膵島周囲の新生血管の経時的変化
東北大学大学院医学系研究科移植再生医学分野
KRP-203 is a Desirable Immunomodulator for Islet Allotransplantation(Transplantation 2021年7月1日)