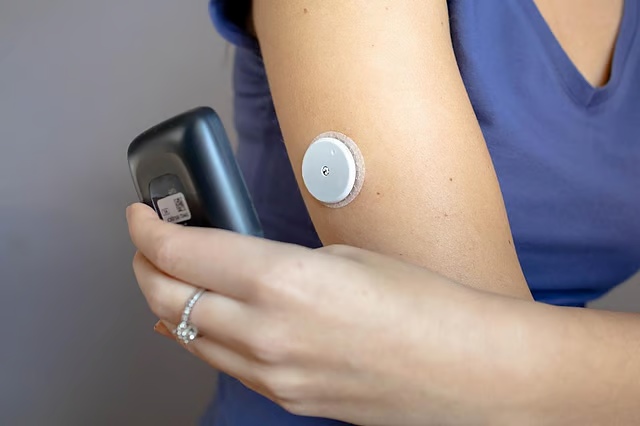
SGLT2阻害薬ジャディアンスが米国で慢性腎臓病の治療薬として承認 CKD患者の腎疾患の進行と心血管死のリスクを低下
SGLT2阻害薬がCKD患者の腎疾患の進行と心血管死のリスクを低下 全入院リスクも低下
ベーリンガーインゲルハイム、イーライリリー・アンド・カンパニーなどは、SGLT2阻害薬ジャディアンス10mg錠(一般名:エンパグリフロジン)について、進行リスクの高い慢性腎臓病(CKD)の成人患者における推算糸球体濾過率(eGFR)の持続的低下、末期腎疾患、心血管死および入院リスクを低下させる医薬品として、米国食品医薬品局(FDA)が承認したと発表した。
第3相臨床試験であるEMPA-KIDNEY試験で、ジャディアンス10mgは、慢性腎臓病の成人患者での腎疾患の進行と心血管死のリスクを有意に低下させたとしている。
同試験は、2型糖尿病の有無を問わない慢性腎臓病の成人患者でのSGLT2阻害薬の臨床試験としては大規模・広範囲の患者層を対象とした臨床試験。参加・除外基準にもとづき、6,600人を超える患者が参加している。
同試験では、標準治療に加えてジャディアンスまたはプラセボを投与し、腎疾患の進行または心血管死を複合主要評価項目として検討された。 *腎疾患の進行は、末期腎臓病(維持透析の開始または腎移植)、eGFRが10mL/min/1.73㎡未満に持続的に低下、腎死、またはランダム割付後にeGFRが40%以上持続的に低下と定義。
その結果、腎疾患の進行または心血管死の相対リスクは、プラセボと比較して28%低減した(絶対リスク減少率は1人年あたり3.6%、HR 0.72、95% CI 0.64~0.82、P<0.0001)。イベント発生率は、ジャディアンス群では13.1%(432/3304)、プラセボ群では16.9% (558/3305)だった。
同試験は、慢性腎臓病でのSGLT2阻害薬の臨床試験としてははじめて、入院(初回入院および再入院)が有意に減少した。入院は主な副次評価項目として試験計画書に規定された項目で、ジャディアンス群ではプラセボ群に比べ入院率が14%低下した(HR 0.86、95% CI 0.78~0.95、p=0.0025)。ジャディアンス群では960人が1,611回入院(24.8件/100人年)したのに対し、プラセボ群では1,035人が1,895回入院(29.2件/100人年)した。
なお、腎機能については、eGFRが20以上45mL/min/1.73㎡未満の患者、およびeGFRが45以上90mL/min/1.73㎡未満で尿中アルブミン/クレアチニン比が200mg/g以上のSGLT2阻害薬による治療に適したと判断した患者を試験の対象とされた。除外基準は、2型糖尿病とアテローム動脈硬化性心血管疾患の既往がありeGFRが60mL/min/1.73㎡未満の患者、1型糖尿病の患者、移植腎をしている・腎移植を予定している患者、透析を受けている患者、多発性嚢胞腎の患者、腎疾患の治療のため免疫抑制剤の静注もしくはプレドニゾン換算で45mgを超えるステロイドの投与を必要とするか、最近投与を受けた患者などとされた。
今回のFDA承認は、EMPOWERプログラムにもとづき、ジャディアンスが取得した4つ目の承認にあたる。世界各地の70万人を超える患者が臨床試験に参加したEMPOWERプログラムは、ベーリンガーインゲルハイムとイーライリリーが心腎代謝疾患の患者の転帰改善に向けた長年にわたる取り組みの一例となっている。
「心不全と2型糖尿病で取得した適応症に続く今回のFDA承認により、腎臓病専門医をはじめとする医師の方々に、進行リスクの高い慢性腎臓病の成人患者でのこの重要な治療選択肢をお届けできるようになった。EUに続いて米国でも同疾患の適応を取得した」と、イーライリリーでは述べている。
腎機能低下・腎不全・心血管死・入院のリスクを下げる新たな選択肢に
なお、日本でのジャディアンス錠の効能・効果は2型糖尿病、慢性心不全であり、心血管イベントおよび腎臓病のリスク減少に関連する効能・効果は取得されていない。また、慢性心不全に対する治療薬として承認されているのはジャディアンス錠10mg。
ジャディアンスのeGFR30mL/min/1.73㎡未満の2型糖尿病患者の血糖コントロール改善を目的とする使用は推奨されていない。同剤の作用機序からみて、こうした患者では効果が得られないおそれがあるとしている。 *高度腎機能障害患者または透析中の末期腎不全患者では同剤の効果が期待できないため投与しないこと。
また、多発性嚢胞腎にともなう慢性腎臓病の患者や、腎疾患のため、免疫抑制薬の静脈内投与もしくはプレドニゾン換算で45mgを超えるステロイドの投与を必要としている患者、もしくはこれらの治療を受けた直後の患者に対するジャディアンスの使用も推奨されていない。これらの患者集団では、ジャディアンスの効果は期待されていないとしている。
ジャディアンスは、1型糖尿病患者の血糖コントロールの改善を目的とする使用は推奨されおらず、1型糖尿病患者に投与した場合、糖尿病性ケトアシドーシスのリスクが上昇するおそれがあるとしている。
「ジャディアンスは、同剤に含まれる添加剤に対し過敏症の既往歴のある患者には投与しないでください。血管浮腫などの過敏症が現れるおそれがある。詳細は、『重要な安全性情報』をご覧ください」としている。
Providence Inland Northwest Healthの研究担当エグゼクティブ・ディレクターで、ヘルスサイエンス研究所の地域担当主席責任医師であり、EMPA-KIDNEYに試験運営医師として携わったワシントン大学医学部教授のKatherine Tuttle氏は、次のように述べている。
「今回の承認により、米国の医療従事者は、慢性腎臓病患者の腎機能低下、腎不全、心血管死や入院のリスクを下げる新たな治療選択肢を得た。第3相臨床試験であるEMPA-KIDNEY試験で明らかにされたジャディアンスの意義あるベネフィットは、米国内の慢性腎臓病の成人患者にとって喜ばしいニュースとなった」。
「慢性腎臓病は、米国の成人の7人に1人以上が罹患しており、うち90%が診断されていない。また、慢性腎臓病は公衆衛生上の危機といえる疾患だが、広く認識されていない。慢性腎臓病の患者にかかる医療費のうち入院費が全体の3分の1~2分の1を占めており、慢性腎臓病が進行すると重篤な心血管系合併症があらわれたり、腎不全に至って透析や移植が必要となることもある」と、ベーリンガーインゲルハイムでは述べている。
関連情報
Empagliflozin in Patients With CKD (American Society of Nephrology (ASN) Congress 2022 - Kidney Week)
Empagliflozin in Patients with Chronic Kidney Disease (New England Journal of Medicine 2023年1月12日)
US FDA approves Jardiance® for the treatment of adults with chronic kidney disease (ベーリンガーインゲルハイム 2023年9月22日)