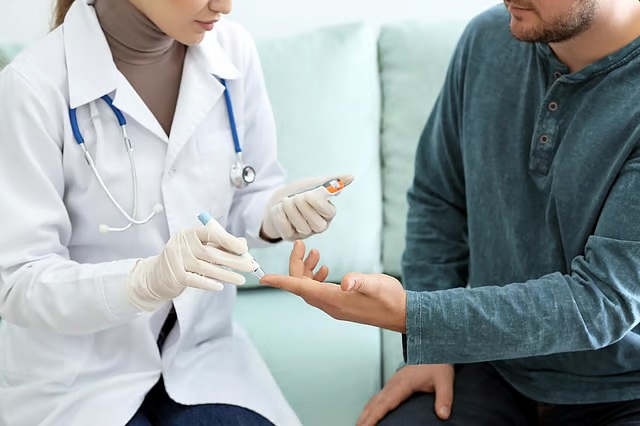
持続皮下センサーと腹腔内インスリンポンプを組合わせた「人工膵臓」を開発中 1型糖尿病患者を負担から解放
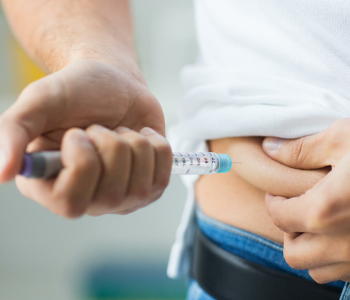
インスリンの腹腔内投与は生理的なインスリン分泌を再現するのに有利
研究は、米イェール大学、イタリアのパドヴァ大学、パヴィア大学らの国際研究グループによるもの。研究成果は、同協会が刊行している「APL Bioengineering」に発表された。
「インスリンの腹腔内投与は、生理的で自然なインスリン分泌を再現するために有利であり、注射やインスリンポンプに比べ、より生理的なインスリン分泌に近付けられると期待している。インスリン投与の遅延が生じない、これまでにない堅牢でシンプルなインスリン治療の実現を目指している」と、パドヴァ大学生物工学部の名誉教授であるClaudio Cobelli氏はコメントしている。
「人工膵臓」とも呼ばれている、インスリンポンプとCGM(持続血糖モニター)を組合せてアルゴリズムにより制御するインスリン自動投与システム(AID)は、患者の糖尿病管理の負担を大幅に軽減するものと期待されている。AIDにより、低血糖のリスクを減らしながら血糖管理を改善し、患者の負担を軽減できることが報告されている。
一方、現在使用されているインスリン自動投与システムは、CGMにより皮下のグルコース濃度を連続して測定し、血糖値を推定するデバイスを組み込んであり、患者は基本的に食事中の炭水化物(糖質)量を把握しシステムに反映させる必要などがある。現状では、CGMによるインスリン感知とインスリン投与のあいだの遅延を避けられないからだ。
このやり方であると、患者の手作業による食事計算などをもとにした操作によりエラーが生じるおそれがあり、システムの動作が不正確になりやすい。さらに高インスリン血症などリスクをゼロにするのは難しいため、患者の大血管疾患などの合併症を完全に防ぐためには、より精度の高いシステムが求められている。
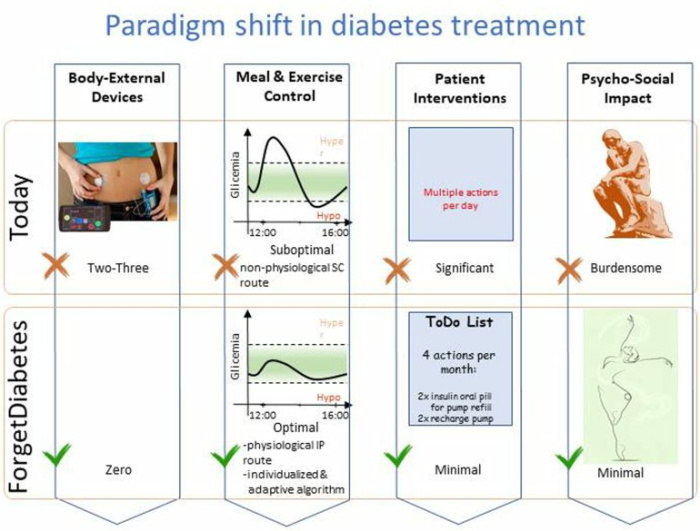
持続皮下インスリンセンサー・腹腔内インスリンポンプ・アルゴリズムを開発
研究グループが開発を進めているのは、持続皮下(SC)インスリンセンサーと腹腔内(IP)インスリンポンプ、それらを制御するコントローラーと高度なアルゴリズムを組合わせたシステム。とくに食事中の糖質の推定値を手動で入力する必要を排除し、糖尿病患者の負担が大幅に軽減できるとしている。
生理的状態では分泌されたインスリンは門脈に流入し肝臓に到達するが、開発中のシステムにより、腹膜腔が仮想コンパートメントとして機能し、腹腔内ポンプによるインスリン送達は、インスリン分泌の生理機能を厳密に模倣していることを実証したとしている。
研究グループは今回、FDAが承認したSCインスリンセンサーとIPインスリンポンプのための1型糖尿病シミュレータを用い、開発したシステムのインスリン動態の2つのコンパートメントモデルの精度を、完全なクローズドループ制御により検証した。
「腹腔内インスリンポンプにより、インスリン送達がより速くなり、食事の影響に自動的に対応しながら血糖コントロールを改善できることが示された。そのために、自然なインスリン動態の特異性に対応できる新しい制御アルゴリズムを開発する必要があった」と、Cobelli氏は述べている。
1型糖尿病は世界中で4,630万人が罹患しており、罹患者数は毎年約3%ずつ増加している。「多くの患者がインスリン必要量を慎重に計算しながら、毎日の注射を行っている。高血糖と低血糖により引き起こされる糖尿病合併症を回避しながら、患者を糖尿病の疾病管理の負担から解放する新しいシステムが望まれている」としている。
Artificial Pancreas Reduces Disease Management Burden for People with Diabetes (米国物理学協会 APL Bioengineering 2023年5月23日)
In silico design and validation of a time-varying PID controller for an artificial pancreas with intraperitoneal insulin delivery and glucose sensing (APL Bioengineering 2023年5月23日)