【新型コロナ】COVID-19ワクチンがついに実用化 米国でも緊急使用許可 ワクチン接種には課題も
2020.12.14
新型コロナウイルス感染症(COVID-19)のワクチンの開発が急ピッチで進められており、ついに実用化された。
英国では、ファイザーとビオンテックの開発した新型コロナウイルスに対するmRNAワクチンが欧米ではじめて承認された。
米国でも、2つのCOVID-19ワクチンが、2020年12月末までに利用可能になる可能性がある。
しかし、新型コロナのワクチンには、安全性と供給量の不足という、大きな課題もある。
英国では、ファイザーとビオンテックの開発した新型コロナウイルスに対するmRNAワクチンが欧米ではじめて承認された。
米国でも、2つのCOVID-19ワクチンが、2020年12月末までに利用可能になる可能性がある。
しかし、新型コロナのワクチンには、安全性と供給量の不足という、大きな課題もある。

新型コロナウイルス感染症(COVID-19)の全世界の感染者数は、2020年12月4日時点で6,504万8,192人、死亡数は150万3,107人に上る。11月9日の時点で感染者数は5,031万人だったので、短期間で急速に増えたことが分かる。 新型コロナの世界中での蔓延を防ぐために、感染を防ぐためのワクチンの開発が急がれている。ワクチンを接種することで、感染症に対する抵抗力(免疫)を高められる。ワクチン製剤の開発は世界中で急速に進められており、12月の時点で実用化の段階に入ってきた。
新型コロナワクチンは実用化の段階に
英国政府は2020年12月2日、ファイザーとビオンテックの開発した新型コロナウイルスに対するmRNAワクチンを欧米ではじめて承認したと発表。同ワクチンの臨床試験データの最終分析で95%の有効性が示されたのを受けたもの。 国民保健サービス(NHS)が準備を進めており、近日中に英国全土で利用できるようになるという。英政府の予防接種合同委員会(JCVI)は、医療機関、高齢者施設、介護施設などで優先的に接種を受けられるよう調整を始めている。 一方、米国のバイオ製薬会社のモデルナが開発中のワクチンも、mRNAワクチンだ。このワクチンも、臨床試験データの最終分析で94%以上の有効性が示された。モデルナは11月末に、このワクチンについて、米食品医薬品局(FDA)に緊急使用許可を申請した。早ければ12月中に利用可能になる可能性がある。 mRNAワクチンは、メッセンジャーRNAを投与するもので、体中でコロナウイルスのタンパク質(抗原)が合成され、免疫が誘導される仕組みになっている。 開発が進められているmRNAワクチンは、有効性を保つために冷凍した状態で運搬や保管をすることが必要だ。モデルナのワクチンは、マイナス20℃で最大半年間の保存が可能で、2℃から8℃では30日間の保存できるとしており、ファイザーとビオンテックのワクチンよりも供給しやすいとみられている。 このほか、英オックスフォード大学とアストラゼネカが共同開発しているウイルスベクターワクチンも、来年1月下旬にも臨床試験の結果が得られ、その後はワクチンの緊急使用許可の申請が出される可能性がある。※米国食品医薬品局(FDA)は12月11日、ファイザーとビオンテックの開発した新型コロナウイルスワクチンについて、緊急使用許可を出したと発表した。臨床試験の結果から、このワクチンを使用する利益が潜在的なリスクを上回っていると判断した。
このワクチンは、4万3,448人を対象に実施した国際共同第3相試験の結果で、95%の有効性が示されており、詳細は医学誌「New England Journal of Medicine」に掲載された。
「緊急許可をサポートするために、このワクチンの安全性、有効性、製造品質について、FDAの厳しい科学的基準を満たしていることを確認するために、オープンで透明なレビュープロセスを実施していきます」と、FDAの生物製剤評価研究センターのビター マークス氏は述べている。
このワクチンは、4万3,448人を対象に実施した国際共同第3相試験の結果で、95%の有効性が示されており、詳細は医学誌「New England Journal of Medicine」に掲載された。
「緊急許可をサポートするために、このワクチンの安全性、有効性、製造品質について、FDAの厳しい科学的基準を満たしていることを確認するために、オープンで透明なレビュープロセスを実施していきます」と、FDAの生物製剤評価研究センターのビター マークス氏は述べている。
日本でもCOVID-19ワクチンの準備が進められている
日本でも12月2日に、予防接種法改正案が成立し、政府はワクチンの確保と接種体制の準備に取り組んでいる。mRNAワクチンは低温で運搬・保管する必要があるので、マイナス70℃やマイナス20℃での保管が可能な冷凍庫の準備も進められている。 COVID-19患者に直接医療を提供する施設の医療従事者や、高齢者や基礎疾患のある人を、接種順位の上位に位置付けて、接種が受けられるようする方針も打ち出された。また、高齢者や基礎疾患のある人などが集団で居住する施設などで働く人や、妊婦の接種順位についても検討されている。COVID-19ワクチンは本当に安全なのか?
一方で、開発された新しいワクチンの安全性を懸念する声もある。一般的に、ワクチン接種では、副反応による健康被害が、稀ではあるものの不可避的に発生するため、日本でも健康被害救済制度が設けられている。 医師からは、「感染予防目的で使うワクチンには、高い安全性が求められる。ワクチン接種により有害事象が起こらないか、安全性の検証には時間がかかる」「mRNAワクチンなど、はじめて使用される種類のワクチンであり、安全性の確認を慎重に行うべきだ」「海外でのデータがそのまま日本人に当てはまらない場合もある」といった声も聞かれる。 新型コロナのワクチンの安全性について、英国糖尿病学会(Diabetes UK)は下記の通りにコメントしている――。
COVID-19ワクチンの開発が急ピッチに進められた背景に、世界中の科学者、政府、製薬企業が1つの共通の目標のために力を集めたことがあります。一方で、ワクチンの開発があまりに急いで行われたため、安全性について懸念している人は少なくありません。
すべてのワクチンの臨床試験は、公正な参加者数が含まれ行われており、その過程で行われるべき作業がスキップされたことはありません。世界的にワクチン開発に共同で取り組んだ結果、資金調達と承認のプロセスが迅速に進められ、ワクチン製造を早期に開始することができるようになりました。
臨床試験には、さまざまな年齢や性別、民族の人や、糖尿病患者を含むさまざまな健康状態にある人が参加しました。英国の医薬品・医療製品規制庁(MHRA)は、導入されたワクチンの安全性を長期にわたり監視し続け、ワクチンが高い基準に適合しているかを確認していきます。
これまで研究で、糖尿病の人のコロナウイルスに対する免疫反応は、糖尿病のない人と変わらないことが分かっています。したがって、ワクチンが糖尿病患者ではうまく作用しないことを示唆する証拠はありません。
なお、COVID-19とインフルエンザの予防接種について、英国公衆衛生サービス(PHE)は、両方のワクチンを接種することについて安全上の懸念はないと述べています。
専門家は、2つのワクチンの間に相互作用があり、適切な作用に影響を与える可能性は低いと考えています。しかしPHEは念のため、COVID-19とインフルエンザのワクチンの接種の間に7日間の間隔を置くことを推奨しています。
日本ではCOVID-19ワクチンの接種に同意している人は7割
世界経済フォーラム(WEF)などが実施した調査によると、新型コロナウイルスのワクチン接種について、「同意する」と答えた人が73%、「同意しない」と答えた人が27%だった。 調査は、WEFとイプソスが10月に、15ヵ国の計1万8,000人超を対象にオンラインで行ったもの。 ワクチン接種について同意しない理由として、「副作用に対する懸念がある」(34%)、「臨床試験の進行が速すぎる」(33%)が挙げられた。 日本では、ワクチン接種に同意するという人は69%で、予防接種を受けないという人では、「副作用への懸念」を挙げた人が62%と多かった。 「COVID-19ワクチンをすべての人が利用可能になったら、3ヵ月以内にワクチン接種を受けたい」と思っている人は、世界の成人の半数(52%)に上った。 日本では「3ヵ月以内にワクチン接種を受けたい」という人は43%、「1年以内」という人は62%だった。 WEFでは「専門家は、COVID-19感染がコミュニティに拡散するのを阻止するために、全人口の70%以上がウイルス対し免疫を獲得する必要があると推定しています。これを達成するために、ワクチン接種は有効な手段になります。ワクチン接種を受けないと、ワクチンは機能しません」と述べている。 「世界保健機関(WHO)も、予防接種に対して抵抗感をもっている人が多いことを、世界の健康に対する脅威のトップ10の1つとして挙げています。予防接種によって感染症を防ぐことは、公衆衛生だけでなく経済活動にも影響し、重要なことです」としている。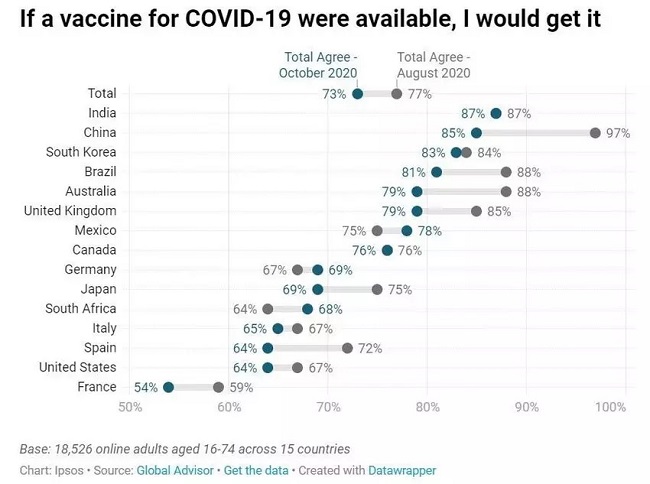
出典:世界経済フォーラム、2020年
今後4〜5ヵ月間は、COVID-19ワクチンの需要は供給を大幅に上回る
COVID-19ワクチンについて、課題はもう1つある。十分な量のワクチンを製造し、ワクチン接種を必要とするすべての人が受けられるよう、公正な手段を確保することだ。 ワクチン開発の専門家として世界的に知られる米ワシントン大学のラリー コーリー氏、ジョンズ ホプキンズ大学のクリス ベイラー氏らは、「このウイルスとの戦いで起こったことは、ワクチン開発のペースが信じられないほど速かったということです。誰もが予想していたよりも、驚くほど速いものでした」と、述べている。 「しかし、ウイルスに対する勝利を宣言するためには、大量のワクチンを製造し、流通させ、さらに接種を実際に受けることが必要となります」。 「2つのCOVID-19ワクチンが2020年12月末までに、米国で利用可能になる可能性がありますが、ワクチン接種の対象となるすべての人に今後数ヵ月で提供するには、ワクチンの数が足りません」としている。 世界のすべての人々の命を救うために、COVID-19のワクチン接種にアクセスできるようにするために、ワクチン製造能力を継続的に拡大することと、入手可能なCOVID-19ワクチンの種類を増やす必要があるという。 「現状ではワクチンの不足は避けられません。安全で効果的なワクチンを製造し供給するのは簡単なことではありません。COVID-19ワクチンは、少なくとも今後4〜5ヵ月間は、需要が供給を大幅に上回るとみられています」としている。米国の成人人口の半分しか接種を受けられない
ファイザーとモデルナのワクチンは、臨床試験で高い有効性が示されているものの、米国では12月に4,000万回の投与しかできず、1月は3,000万回、2月は4,000万回、3月と4月は6,000万の投与ができると見込まれている。 ワクチンはそれぞれ2回の接種が必要であり、2億回の接種に達したとしても1億人しかカバーできず、これは米国の成人人口の半分に過ぎないという。 医療機関、高齢者施設、介護施設などで優先的に接種を受けられるよう調整し、直接医療を提供する医療従事者や、高齢者や基礎疾患のある人などを、接種順位の上位に位置付ける必要がある。 医療施設や高齢者施設などで従事する人をはじめ、高齢者などと接する機会が多い職種の人を優先することも考えられるとしている。 新型コロナウイルス感染症のワクチンについて(厚生労働省)ジョンズ ホプキンス大学 コロナウイルス リソース センター
The Coming Covid-19 Vaccine Scarcity(ジョンズ ホプキンス大学 2020年12月3日)
UK authorises Pfizer/BioNTech COVID-19 vaccine(英国政府 2020年12月2日)
FDA Takes Key Action in Fight Against COVID-19 By Issuing Emergency Use Authorization for First COVID-19 Vaccine(米国食品医薬品局 2020年12月11日)
Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine(New England Journal of Medicine 2020年12月10日)
Coronavirus Vaccines And Diabetes(英国糖尿病学会 2020年12月2日)
Moderna Announces Primary Efficacy Analysis in Phase 3 COVE Study for Its COVID-19 Vaccine Candidate and Filing Today with U.S. FDA for Emergency Use Authorization(モデルナ 2020年11月30日)
Fewer people say they would take a COVID-19 vaccine now than 3 months ago(世界経済フォーラム 2020年11月5日)
[Terahata / 日本医療・健康情報研究所]