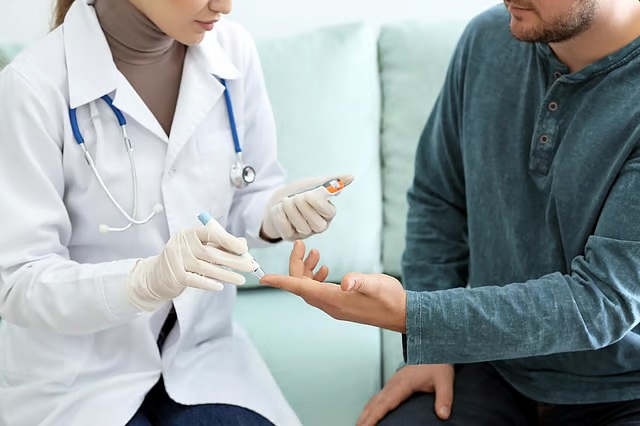
糖尿病合併の認知症を簡単に予測できる血液バイオマーカーを発見 認知症リスクの高い患者を早期発見し予防介入
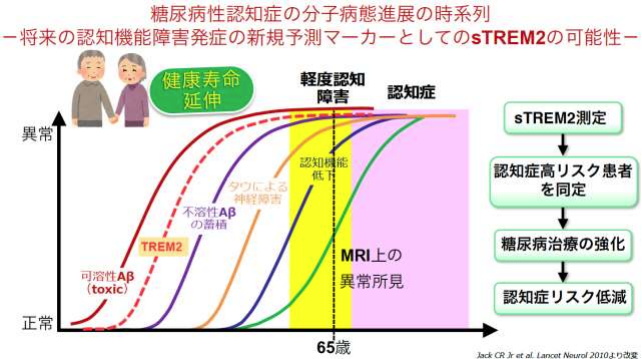
血中sTREM2で糖尿病患者の認知症発症を早期に予測
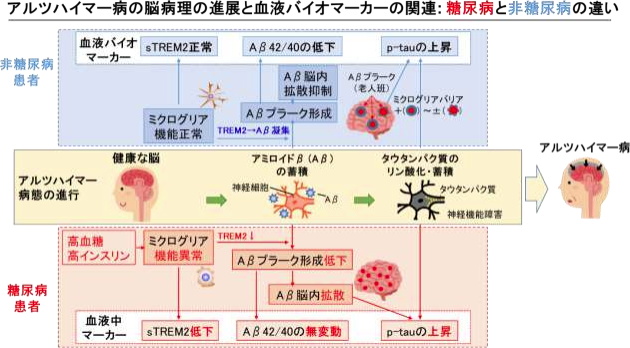
京都医療センターなどは、多項目血液バイオマーカーの包括的な解析により、糖尿病患者では認知機能が正常な時期から、脳内のミクログリア機能の低下を示唆する血中sTREM2の低下が最初に出現することを、世界ではじめて明らかにした。
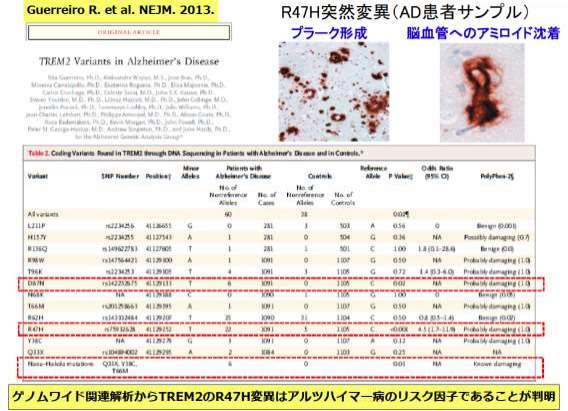
TREM2は、脳のミクログリアにあるタンパク質で、アルツハイマー病の発症リスクに関わる遺伝子のひとつ。タンパク分解により切断され、可溶型のsTREM2として、脳脊髄液や血液に分泌される。アルツハイマー病患者の脳脊髄液では、sTREM2の濃度が増加しており、さらにTREM2遺伝子のR47HおよびR62H変異は、アルツハイマー病発症リスクの上昇に関連している。
さらに、アルツハイマー病の多項目バイオマーカーを血液で解析することで、糖尿病患者では、脳内でのアミロイドβ(Aβ)タンパク蓄積を反映する血中Aβ42/40比の低下を認めないにもかかわらず、その下流にある脳内タウタンパク蓄積を反映する血中リン酸化タウ(pTau)タンパクの上昇を認められた。
Aβ(アミロイドβ)タンパクとリン酸化タウタンパク(pTau)は、いずれもアルツハイマー病患者の脳に異常に蓄積する病因タンパク質。この2つのタンパク質が、それぞれ細胞外、細胞内に蓄積することが、アルツハイマー病の病理学的な特徴となる。
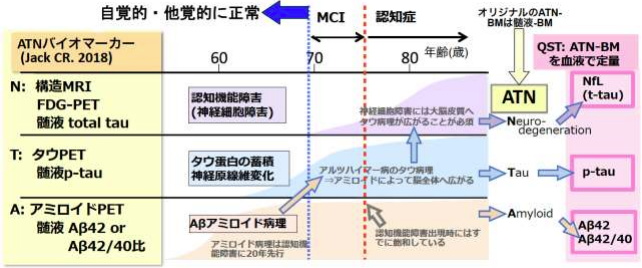
最近では、PET検査でAβやリン酸化タウタンパクの蓄積を同定した患者で、Aβ、リン酸化タウを血液中で測定して比較することで、血液バイオマーカーによっても脳内にこれらの蓄積タンパクがあるかどうかを判定できるようになっている。
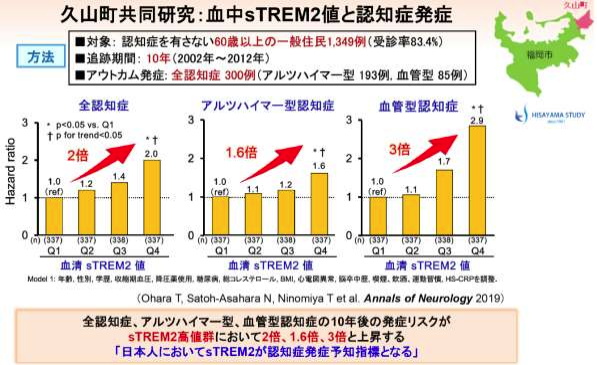
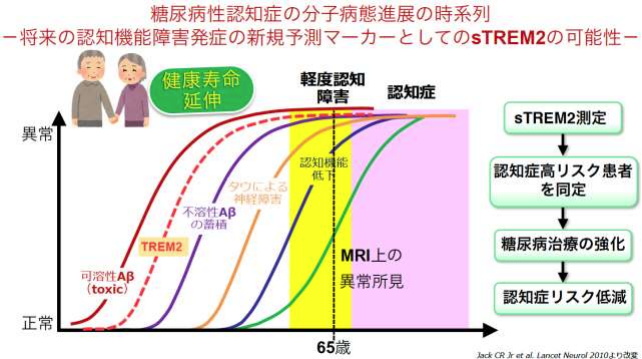
sTREM2は血液バイオマーカーとして有用
近年の疫学研究で、糖尿病は脳血管性認知症のリスクであるだけでなく、アルツハイマー病の発症リスクを2倍以上、上昇させると報告されている。認知機能低下は、糖尿病治療の遵守や患者の健康寿命に悪影響を及ぼすため、糖尿病患者での認知症対策は喫緊の課題であり、認知症未発症段階での糖尿病患者の適切な管理と予防のためには、どのような糖尿病患者が認知症を発症するかを予測する非侵襲的で簡便な血液バイオマーカーの開発が急務となっている。
研究成果は、糖尿病性認知症の発症・進展機序の解明につながるもので、血中sTREM2の測定は、認知症発症リスクの高い糖尿病患者を認知症発症以前の超早期に、簡便かつ客観的に同定することができる血液バイオマーカーとして有用と考えられるとしている。さらに、糖尿病患者で血中sTREM2が高値の患者を対象に予防的介入を行うことで、認知症リスク低減に寄与できる可能性が期待されるとしている。
「今回の研究により、糖尿病性認知症という疾患単位を規定する特徴的なバイオマーカーの時系列変化をはじめて明らかにしました。糖尿病患者で認められる血液バイオマーカー変化の時系列、すなわちsTREM2の低下からはじまり、その後にAβ42/40比の低下をともなわないpTau上昇を呈することを示し、脳内のミクログリア機能の低下が糖尿病性認知症の発症機序カスケードの最上流にあり、それに続くアルツハイマー病理変化の発現様式に影響を与えるという仮説をはじめて提唱しました」と、研究グループでは述べている。
研究は、京都医療センター臨床研究センターの浅原哲子部長、同山陰一主任研究員、健康科学大学の田中将志教授、京都認知症総合センタークリニックの秋口一郎所長、川崎照晃院長、量子科学技術研究開発機構(QST)の徳田隆彦医長らの研究グループによるもの。研究成果は、「Diabetes Research and Clinical Practice」にオンライン掲載された。
糖尿病患者47人と非糖尿病患者74人を対象に血中sTREM2を測定
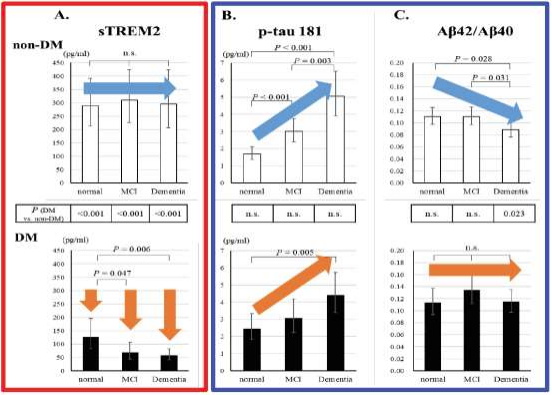
研究グループは今回の研究で、脳内の老廃物などを掃除するミクログリア細胞の機能を反映する血中sTREM2および世界標準となっているアルツハイマー病の多項目血液バイオマーカー(Aβ42/40比、pTau、ニューロフィラメント軽鎖(NfL)など)を測定して、患者の認知機能障害の程度により分類した正常群・軽度認知障害群・認知症群の間で、これらの血液バイオマーカーの変動を解析した。
その結果、糖尿病の認知症発症をもっとも早期に反映する指標は、血液中のsTREM2の減少である可能性を、世界ではじめて明らかにした。さらに、糖尿病患者では、sTREM2の低下の後に続く変化として、脳内でのAβタンパク蓄積を反映する血中Aβ42/40比の低下を認められないにもかかわらず、その下流にあって神経細胞障害に直結する脳内タウタンパク蓄積を反映する血中pTauの上昇が認められた。
研究グループは今回の研究で、京都認知症総合センタークリニックで経過観察と加療を受けている糖尿病患者(47人)と非糖尿病患者(74人)を対象に、糖尿病の病歴と経過、認知機能検査、画像診断などの臨床情報を収集し、また保存されていた血液検体を用いて、ミクログリアの機能を反映する血中sTREM2およびアルツハイマー病の多項目血液バイオマーカー(ATNバイオマーカー: Aβ42/40比、pTau、NfLなど)を測定した。
患者の認知機能障害の程度により分類した正常群・軽度認知障害群・認知症群の間で、これらの血液バイオマーカーの変動を解析した。sTREM2の測定はa RayBiotech Human TREM-2 ELISA法で行った。
ELISA法は、試料溶液中に含まれている目的の抗原(アルツハイマー病なら原因タンパクであるAβやリン酸化タウなど)を、その抗原を特異的に認識する特異抗体で捕捉するとともに、酵素反応を利用して検出・定量する方法。
ミクログリアの機能低下がアルツハイマー病の病態進行の鍵に
アルツハイマー病では、脳の中で作られた可溶性の毒性Aβタンパクが、タウタンパクのリン酸化と細胞内への蓄積を引き起こし、そのリン酸化タウタンパクが大脳皮質に広がることにより、大脳の神経細胞が広汎に障害されて、認知症を発症すると考えられている。
そのため、可溶性の毒性Aβが脳全体に拡散しないように、通常の病初期にはミクログリアという細胞が働いて、Aβを不溶化して局所(老人斑と呼ばれる異常構造物)に閉じ込め、さらにミクログリアが老人斑周囲を取り囲みAβの拡散を防ぐ「バリア」となって、周囲の脳組織を保護していると考えられている。
加齢などにより、このアルツハイマー病の病初期に働くミクログリアの保護的な活動が低下すると、Aβの拡散からリン酸化タウの誘導、細胞障害というアルツハイマー病理の進展カスケードが作動してしまう。
ミクログリアに発現しているTREM2の遺伝子変異(TREM2の機能が低下)は、アルツハイマー病の発症リスクを上げることも報告されている。TREM2はその一部が可溶型TREM2(sTREM2)として放出され、そのsTREM2の量はミクログリアの活性化状態を反映しており、sTREM2はヒトの脳脊髄液および血液中でも定量することができる。
一方、糖尿病患者に出現する「糖尿病性認知症」では、アルツハイマー病とは異なる脳病理の特徴が、羽生氏らによるPET検査を用いた研究により報告されている。アルツハイマー病の最初期病変である老人斑(Aβ蓄積から構成)の形成がわずかである一方で、Aβの下流にあるリン酸化タウタンパク質は蓄積し、認知機能が低下するという。
アルツハイマー病関連バイオマーカーは、ヒト血液中に極微量しか存在せず、従来は測定ができなかったが、近年に開発された超高感度デジタルELISAマシンSimoaを使用することで、アルツハイマー病のコア・バイオマーカーであるATNバイオマーカーのすべてが測定可能になった。
バイオマーカーの観点からミクログリアの機能低下を推定
すでに臨床的・画像診断的観察から提唱されていた「糖尿病性認知症」の病態、すなわち「脳内のAβアミロイドの沈着が少ないにもかかわらずタウ病理が出現する」という仮説について、今回の研究により、バイオマーカーの観点からAβとタウの上流にミクログリアの機能低下という病態を推定することで、そのような「糖尿病性認知症」の脳病態を説明することが可能になった。
「糖尿病性認知症」については、これまでどのよう分子機構でそのような病態が出現するのかが明らかではなく、根本的にそのような病態があるのかということにも疑念を呈する意見もあったが、今回の研究で、「糖尿病性認知症」の発症病態の仮説を体系化することができたとしている。
「今後、糖尿病性認知症は、アルツハイマー病とも連続する新しい認知症の原因疾患のひとつとして、より大規模な臨床研究やモデル動物などの基礎研究により、その疾患概念が確立されていく可能性があり、我々の研究結果はその扉を開いたと考えています。今後、さらなる研究で、糖尿病性認知症の効果的な予知指標・診断法・治療戦略の開発に取り組んでいきたいと考えています」と、研究グループでは述べている。
国立病院機構京都医療センター 臨床研究センター 内分泌代謝高血圧研究部
Soluble TREM2 and Alzheimer-related biomarker trajectories in the blood of patients with diabetes based on their cognitive status (Diabetes Research and Clinical Practice October 2022年10月19日)