週1回投与のデュアルGIP/GLP-1受容体作動薬「Tirzepatide」 成人2型糖尿病患者のHbA1c・体重減少で優越性を示す
Tirzepatideの最高用量(15mg)群で、2.46%のHbA1c低下および12.4 kg(13.1%)の体重減少が示され、セマグルチド1mg投与群と比べ2倍の体重減少が認められた。

週1回投与のデュアルGIP/GLP-1受容体作動薬「Tirzepatide」
「Tirzepatide」は、2型糖尿病治療のために開発されている新しいクラスの治療薬。グルコース依存性インスリン刺激性ポリペプチド(GIP)とグルカゴン様ペプチド(GLP-1)の両インクレチンの作用を単一分子に統合した、新規の週1回投与デュアルGIP/GLP-1受容体作動薬だ。
GIPは、GLP-1受容体作動薬の効果を補完するホルモン。前臨床モデルで、GIPは食物摂取量を減少させエネルギー消費を増加させることが示されているため、体重の減少をもたらすと考えられる。また、GLP-1受容体作動薬と併用することでグルコースと体重に対してより大きな効果をもたらす可能性がある。Tirzepatideは、成人2型糖尿病患者の血糖値管理と慢性的体重管理のために第3相で開発中。また、非アルコール性脂肪肝炎(NASH)の治療薬としても研究されている。
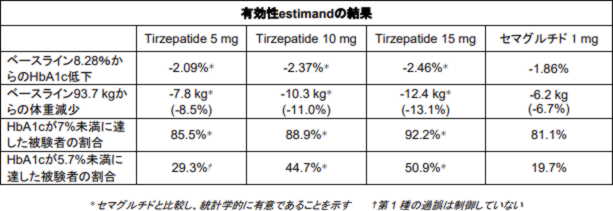
現時点でSURPASSプログラム最大にあたるSURPASS-2試験のトップライン結果では、有効性estimandを用いた評価から、Tirzepatide最高用量群(15mg)で、2.46%のHbA1c低下および12.4kg(13.1%)の体重減少が示された。セマグルチド群の1.86%のHbA1c低下および6.2kg(6.7%)の体重減少に対し、Tirzepatideの最低用量(5mg)群では、2.09%のHbA1c低下および7.8kg(8.5%)の体重減少が示された。
さらに、糖尿病ではない人のレベルであるHbA1c 5.7%未満に到達した患者の割合は、セマグルチド群の20%に対し、Tirzepatide最高用量群(15mg)では51%だった。Tirzepatideの全体的な安全性プロファイルはこれまでに報告されたSURPASS試験および確立されたGLP-1受容体作動薬と同様だった。各投与群ともに消化器系の副作用がもっとも多く報告された有害事象だった。
米国National Research Instituteの医長でSURPASS-2試験の治験責任医師であるJuan Pablo Frías氏は次のように述べている。
「直接比較試験は臨床医が治験薬の有効性を評価するための有効な判断基準です。2型糖尿病治療薬として承認されている最高用量のセマグルチドと比較した本試験結果は、Tirzepatideの3用量全ての群の優れたHbA1c低下と体重減少を示しています。新しい治療選択肢は2型糖尿病患者さんのHbA1cおよび体重減少の目標達成に貢献できる可能性があります。TirzepatideはSURPASS-2試験において、既存のGLP-1受容体作動薬でこれまでに確認された以上の有効性を示しました」。
2型糖尿病のHbA1cおよび体重減少の目標達成に貢献できる可能性
SURPASS-2試験は、メトホルミンの追加療法として成人2型糖尿病患者を対象に、Tirzepatideとセマグルチドの有効性および安全性を比較した40週間の無作為化非盲検試験。被験者1,879人の糖尿病の平均罹病期間は8.6年、ベースラインのHbA1cは8.28%、ベースラインの体重は93.7kgだった。
有効性estimandおよび治療方針estimandを用いた評価では、HbA1c低下と体重減少について、Tirzepatideの3用量(5mg、10mg、15mg)全群のセマグルチド群に対する優越性が示された。糖尿病患者に米国糖尿病学会が推奨する目標であるHbA1c 7%未満に到達した患者の割合は、セマグルチド群の81%に対し、Tirzepatide最高用量群(15mg)では92%だった。
治療方針estimandを用いた評価では、HbA1c低下および体重減少について、Tirzepatideの3用量(5mg、10mg、15mg)全群のセマグルチド1mgに対する優越性が示された。HbA1c 7%未満に到達した被験者の割合はセマグルチド群に対し、Tirzepatideの3用量(5mg、10mg、15mg)全群で数値的に多く示された。セマグルチド群に対する有意差はTirzepatide5mg群では認められず、Tirzepatide10mg群およびTirzepatide15mg群で認められた。
具体的な詳細は以下の通り――。
⚫ HbA1c低下:-2.01%(5mg)、-2.24%(10mg)、-2.30%(15mg)、-1.86%(セマグルチド1mg)
⚫ 体重減少:-7.6kg(5mg)、-9.3kg(10mg)、-11.2kg(15mg)、-5.7kg(セマグルチド1mg)
⚫ HbA1cが7%未満:82.0%(5mg)、85.6%(10mg)、86.2%(15mg)、79.0%(セマグルチド1mg)
⚫ HbA1cが5.7%未満:27.1%(5mg)、39.8%(10mg)、45.7%(15mg)、18.9%(セマグルチド1mg)
54mg/dL未満の低血糖はTirzepatide投与群で0.6%(5mg)、0.2%(10mg)、1.7%(15mg)に認められ、セマグルチド群で0.4%に認められた。
各投与群ともに消化器系の副作用がもっとも多く、悪心(17.4%(5mg)、19.2%(10mg)、22.1%(15mg)、17.9%(セマグルチド))、下痢(13.2%(5mg)、16.4%(10mg)、13.8%(15mg)、11.5%(セマグルチド))、嘔吐(5.7%(5mg)、8.5%(10mg)、9.8%(15mg)、8.3%(セマグルチド))が認められた。
有害事象に起因する治療中止割合は、5.1%(5mg)、7.7%(10mg)、7.9%(15mg)、3.8%(セマグルチド)だった。
SURPASS-2試験の完全なデータはまだ評価されていないが、第81回米国糖尿病学会年次学術集会で公表され、2021年に論文化される予定としている。













