「ケトン体」に糖尿病性腎臓病に対する腎臓保護の秘めた⼒が 臓器を守る新たな治療標的となる可能性 SGLT2阻害薬の腎臓保護作⽤の⼀端を解明
2020.08.07
滋賀医科⼤学は、ケトン体が糖尿病から腎臓を守る新たな治療標的となる可能性があることを、糖尿病モデルマウスを⽤いた検討により発⾒したと発表した。
ケトン体はSGLT2阻害薬の腎臓保護メカニズムの⼀端を担っている
これまで糖尿病患者の急性合併症として知られているケトアシドーシスの原因物質としてネガティブなイメージが根付いていたケトン体に、糖尿病による臓器障害を予防しうる秘めたる⼒があるという、糖尿病治療におけるケトン体の位置づけにパラダイムシフトを起こす結果が、糖尿病性腎臓病モデルマウスを⽤いた今回の研究により導き出された。 ケトン体の効果は、近年類をみない腎予後改善効果を発揮しているSGLT2阻害薬の腎臓保護メカニズムの⼀端を担っていることも明らかにした。糖尿病性腎臓病は日本の透析導⼊原疾患1位の疾患であり、新たな治療法の開発が望まれている。ケトン体のもつ臓器保護効果には、今後の糖尿病性腎臓病克服への期待をもてるとしている。 研究は、滋賀医科⼤学糖尿病内分泌・腎臓内科の富⽥⼀聖⼤学院⽣、久⽶真司学内講師、前川聡教授らを中⼼とする多施設共同研究グループによるもの。研究成果は、学術誌「Cell Metabolism」に掲載された。ケトン体に糖尿病性腎臓病の悪化を抑制する秘めたる⼒が
ヒトの体を構成する細胞は常にATPを産⽣し、その⽣命、機能を維持している。研究グループは以前より、糖尿病性腎臓病の腎臓ではこのATP産⽣が障害されることで、腎臓病が進展するという結果を⾒出し、その是正による新規治療の開発を⽬指して研究を進めてきた。 細胞がATPを作るために必要な材料は主にブドウ糖、脂肪酸、ケトン体だ。この中でもケトン体は、⻑期絶⾷中のATP産⽣源としての役割が強く、飽⾷の時代でその必要度は減り、さらに糖尿病の急性合併症であるケトアシドーシスの原因物質となることから、強いネガティブイメージが根付いていた。 一方、近年、腎臓から尿へのブドウ糖排泄を増加させて⾎糖値を低下させるSGLT2阻害薬が新規糖尿病治療薬として臨床応⽤された。同剤には⾎糖値を低下させる効果だけでなく、既存の糖尿病治療薬にはみられない強い腎臓保護効果があることが分かってきた。 興味深いことに、このSGLT2阻害薬を内服した患者の⾎中では、絶⾷と同じようにケトン体濃度が少し上昇することが報告され、これらは他の糖尿病治療薬にはみられない現象だ。 そこで研究グループは、⻑くネガティブイメージが根付いたケトン体には、腎臓のエネルギー代謝異常を是正し、糖尿病性腎臓病の悪化を抑制しうる秘めたる⼒があるのではないかと考え、マウスモデルを⽤いてこの仮説を検証した。⾎中のケトン体が糖尿病性腎臓病の改善に有効である可能性
その結果、主に次のことが明らかになった――。 (1) 糖尿病性腎臓病の腎臓はATP産⽣にケトン体を必要としている 腎臓を構成する細胞のひとつ近位尿細管細胞は、元来、ATP産⽣に脂肪酸を利⽤するとされていたが、今回の研究で、糖尿病性腎臓病モデルマウスの近位尿細管細胞では脂肪酸由来のATP産⽣が障害される⼀⽅で、ケトン体由来のATP産⽣が増強するという結果が得られ、障害された腎臓ではATP産⽣が脂肪酸依存からケトン体依存に変化することが明らかになった。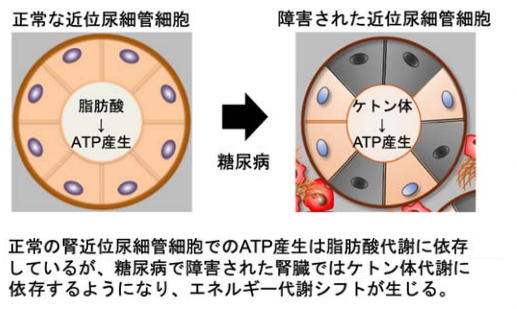
出典:滋賀医科⼤学糖尿病内分泌・腎臓内科、2020年
(2) ケトン体前駆物質(1,3-ブタンジオール)はマウス糖尿病性腎臓病を改善させる
糖尿病性腎臓病モデルマウスにケトン体前駆物質である1,3-ブタンジオールを投与することで、腎内ATP産⽣の回復、腎障害の改善が確認された。これらの結果から、ATP産⽣源としてケトン体を要求する障害腎に対し、ケトン体を供給することが、まさに腎臓病の改善につながる可能性が⽰された。この結果は、ケトン体代謝の制御が糖尿病性腎臓病の治療につながる世界ではじめての知⾒となる。
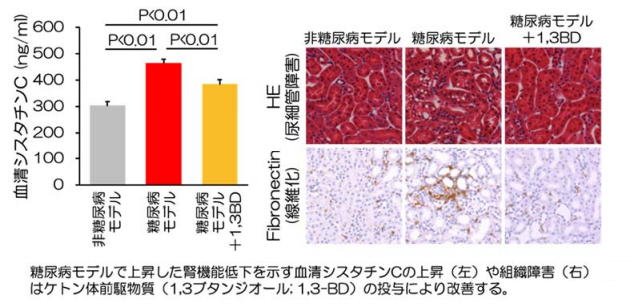
出典:滋賀医科⼤学糖尿病内分泌・腎臓内科、2020年
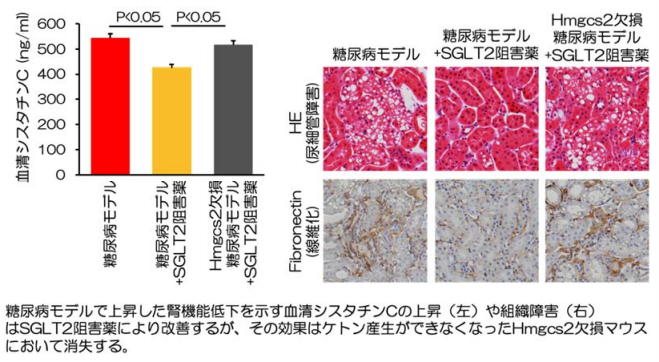
(3) ケトン体の産⽣障害によりSGLT2阻害薬による腎臓保護効果は打ち消される
SGLT2阻害薬の腎臓保護作⽤にケトン体が関与するか否かを検証するために、内因性ケトン産⽣に必要な律速酵素Hmgcs2を⽋損させた糖尿病性腎臓病モデルマウスを作製し、SGLT2阻害薬(エンパグリフロジン)の効果を検証したところ、同マウスでは、SGLT2阻害薬の腎保護効果が消失した。これにより、SGLT2阻害薬の腎臓保護効果に内因性のケトン体産⽣が不可⽋であることを証明され、世界中でその解明が進められているSGLT2阻害薬による臓器保護機構の⼀端を解明する結果となった。
出典:滋賀医科⼤学糖尿病内分泌・腎臓内科、2020年
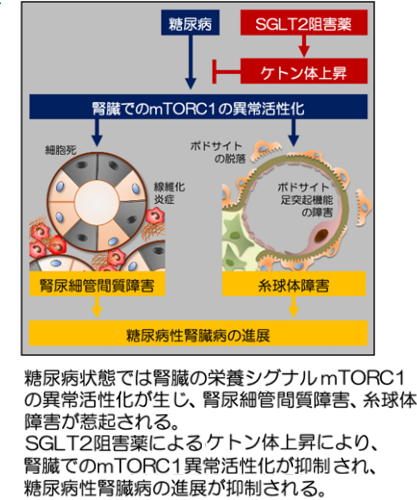
(4) 栄養感知シグナルmechanistic target of rapamycin complex 1(mTORC1)の抑制がケトン体による腎臓保護機構の標的である
細胞には細胞外の栄養状況の変化を感知し、細胞の機能変化をもたらすシステムが備わっており、過栄養、低栄養に応じて細胞⽣命活動を維持できるようになっている。その栄養感知シグナルのひとつにmTORC1という過栄養を感知するシグナルが存在しているが、このmTORC1が糖尿病性腎臓病の腎臓では異常活性化しており、この異常活性化が、尿細管細胞障害、⽷球体障害を引き起こしていることが分かっている。研究グループは今回、ケトン体は絶⾷シグナルとしてmTORC1シグナルを抑制し、糖尿病性腎臓病に対する腎臓保護をもたらすことを明らかにした。
出典:滋賀医科⼤学糖尿病内分泌・腎臓内科、2020年
ケトン体を標的とした糖尿病合併症治療を発展させていく必要が
研究グループは今回、マウスモデルを⽤いた研究から、⾎中のケトン体濃度を適切に上昇させることが糖尿病性腎臓病の改善に有効となる可能性を世界ではじめて証明した。 糖尿病の急性合併症であるケトアシドーシスの原因物質となることから陰のイメージが根付いていたケトン体には、単なる絶⾷期間中のエネルギー源としてだけでなく、糖尿病にともなう臓器障害に対する組織修復能⼒が備わっていることが明らかになった。 飽⾷の時代になり、その必要性が失われ、我々の⾎液から消えることとなったケトン体が、SGLT2阻害薬により呼び戻され、臓器保護の観点から脚光を浴びる可能性が⽰された。 ケトン体を上昇させる⽅法として、今回使⽤したケトン体前駆物質(1,3-BD)、SGLT2阻害薬に加え低糖質⾷(ケトン⾷)などがあるが、ケトン体代謝以外の代謝には差異があるため、臓器保護に対しては異なる結果を⽣み出す可能性もある。 よって今後は、「単に⾎中のケトン体濃度を上げることを⽬的にするだけでなく、ケトン体のもつ臓器保護という陽の側⾯をより安全に引き出すための⼿段を⾒出すことで、ケトン体を標的とした糖尿病合併症治療を発展させていく必要がある」と、研究グループは述べている。 滋賀医科⼤学糖尿病内分泌・腎臓内科SGLT2 Inhibition Mediates Protection from Diabetic Kidney Disease by Promoting Ketone Body-Induced mTORC1 Inhibition(Cell Metabolism 2020年7⽉28⽇)
関連情報
- SGLT2阻害薬を使用している2型糖尿病患者でケトアシドーシスのリスクが3倍に上昇 41万例超を調査
- 血中ケトンを「迅速」に「定量」できることをご存じですか?
糖尿病ケトアシドーシス(DKA)における救急時の迅速診断と経過観察に有用
[Terahata / 日本医療・健康情報研究所]