糖尿病の膵β細胞オートファジーの変化を明らかに インスリン抵抗性が膵β細胞のオートファジー活性を不均一化
膵β細胞のオートファジーの変化を蛍光プローブで評価
研究は、順天堂大学大学院医学研究科代謝内分泌内科学の青山周平助教、西田友哉准教授、綿田裕孝教授、群馬大学・北里大学・新潟大学の共同研究グループによるもの。研究成果は、「Cell Chemical Biology」にオンライン掲載された。 オートファジーは、細胞の機能維持に不可欠なタンパク質分解系であり、インスリンを分泌する膵β細胞の機能維持にも寄与していると考えられている。
日本人の2型糖尿病の多くで、血糖値を低下させるインスリンを分泌する膵β細胞の機能不全が認められる。糖尿病に関連して、オートファジーの活性の変化や制御機構を理解することは、糖尿病治療法の開発に大きく貢献するとみられる。
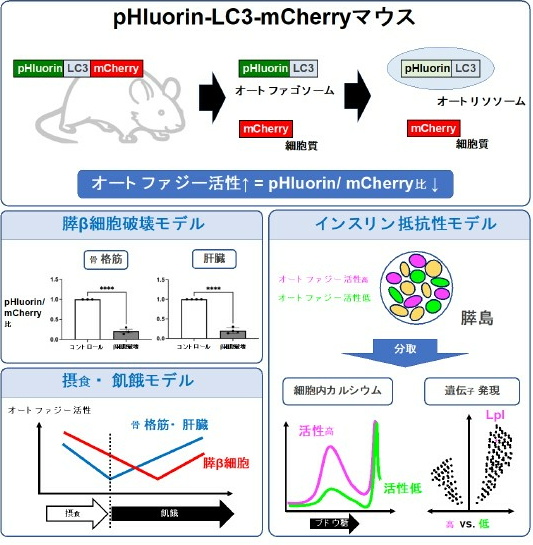
これまで、生体内でオートファジーを正確に評価するのは困難だった。そこで、研究グループは今回、蛍光タンパクを利用したオートファジー活性を評価できるタンパクであるpHluorin-LC3-mCherryを全身で発現するpHluorin-LC3-mCherryマウスを作製し、糖尿病の病態で膵β細胞を中心にその活性や機能の変化、遺伝子発現の変化の解析を行った。
このマウスは、オートファジー活性(オートファジーフラックス)を評価できる蛍光プローブを全身で発現する。蛍光プローブは、蛍光を利用して測定に用いるタンパクで、今回は、オートファジーの活性を定量評価できるタンパクとして利用した。
オートファジーが活性化されると、このプローブはpHluorin-LC3とmCherryに切断され、前者はオートファジーにより分解されるため、pHluorin/mCherryの蛍光強度の比が低下する。
糖尿病マウスでは膵β細胞のオートファジーの活性が不均一
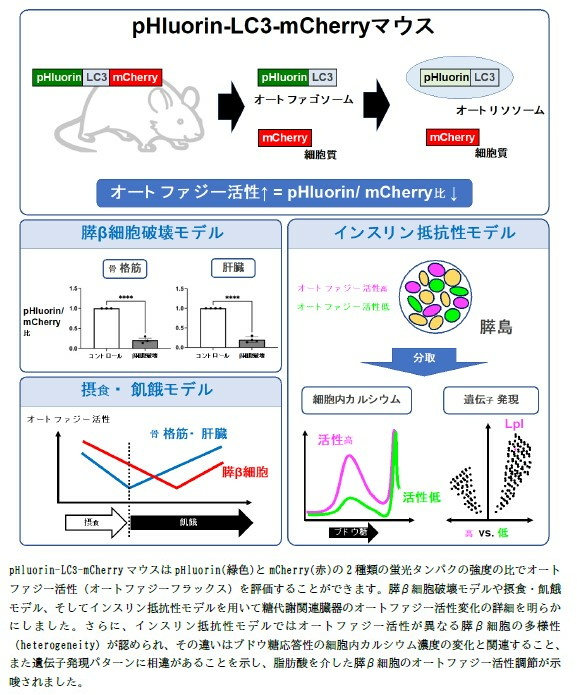
研究グループは、このマウスから採取した胎児線維芽細胞は、アミノ酸飢餓刺激によりpHluorin/mCherry比が低下することを確認。さらに、飢餓刺激により肝臓や骨格筋といった臓器でpHluorin/mCherry比が低下することから、マウスでもオートファジー活性を正しく評価できると考えた。 さらに、糖尿病モデルである膵β細胞破壊マウスでは、インスリンの不足により著明な高血糖をきたすとともに、インスリンの作用臓器である肝臓や骨格筋でオートファジーが活性化され、それにともないpHluorin/mCherry比が低下することを明らかにした。
一方で、糖尿病の発症で重要なインスリン抵抗性がみられるモデルマウスでは、膵β細胞のオートファジーの活性が一律な変化をみせず、活性が低下したβ細胞や上昇したβ細胞の出現が明らかとなり、不均一性(heterogeneity)が顕在化した。
これまで均一な細胞集団と考えられていた健常・病的なさまざまな組織で、機能的・形質的に不均一性があることが分かり、注目されている。
これらの機能的な違いを検討するため、膵β細胞をオートファジー活性の高い細胞と低い細胞に分けて採取し、ブドウ糖応答性細胞内カルシウム流入の変化を調べた。
膵β細胞は、細胞外のブドウ糖濃度の上昇を感知し、細胞内にカルシウム流入が引き起こされた結果、インスリンを分泌する。
その結果、オートファジー活性の高い細胞では細胞内カルシウム流入が大きいことが観察され、インスリン分泌能も高いと考えられた。
今後は膵β細胞のオートファジーの不均一性や、脂肪酸代謝との関連を解明
さらに、これらの活性が異なる膵β細胞の特徴を明らかにするため、mRNAシークエンスによる網羅的遺伝子発現解析、および質量分析法によるプロテオーム解析を行った。 その結果、オートファジー活性の高い細胞では中性脂肪を分解し遊離脂肪酸に替えるのに重要なリポタンパクリパーゼの発現が上昇していることを見出した。
膵β細胞ではオートファジーの活性が、インスリンよりも遊離脂肪酸の濃度変化に関係していると考えられること、また、脂肪酸により膵β細胞のオートファジー活性が上昇することをふまえると、リポタンパクリパーゼを介した脂肪酸が膵β細胞のオートファジー活性の調節をになっていることが想定された。
「今回、これまで正確に評価されていなかった糖尿病病態に関連する膵β細胞のオートファジー活性の変化を報告しました。オートファジーの活性に不均一性が認められること、その不均一性が膵β細胞の機能と深く関連していること、そしてその調節に脂肪酸が関与している可能性があることを明らかにしました」と、研究グループでは述べている。
「今後は、オートファジーの不均一性がもつ機能的な意義、特に脂肪酸代謝と関連したその顕性化のメカニズムを明らかにし、糖尿病の病態の解明とその制御による治療法の開発につなげたいと考えています。また、pHluorin-LC3-mCherryマウスは全身でのオートファジー活性評価に応用できることから、このマウスを用いて2型糖尿病に関連した膵島以外の糖代謝関連臓器での詳細な検討を行うこと、さらに糖尿病以外のさまざまな疾患でオートファジーがもつ意義を解明することを計画しています」としている。
順天堂大学大学院医学研究科代謝内分泌内科学
Monitoring autophagic flux in vivo revealed its physiological response and significance of heterogeneity in pancreatic beta cells (Cell Chemical Biology 2023年3月20日)