膵臓部分切除術後の糖尿病発症に関与する因子を解明 腸内環境と膵臓内分泌細胞の可塑性が重要 九州大学、国立国際医療研究センターなど
膵臓部分切除術後の糖尿病の発症予測とともに、糖尿病発症での腸内環境と膵内分泌細胞の可塑性の病態生理的意義を臨床的に証明した。研究成果は、膵臓部分切除術後のみならず、通常の2型糖尿病の発症メカニズムの理解にも新しい洞察をもたらすものだ。

膵臓部分切除術後の糖尿病発症の発症率 PDとDPとでは大きな差が
研究は、九州大学大学院医学研究院病態制御内科学(第三内科)の小川佳宏教授や、国立国際医療研究センター研究所糖尿病情報センターの坊内良太郎室長、東京医科歯科大学大学院医歯学総合研究科分子内分泌代謝学分野(糖尿病・内分泌・代謝内科)の山田哲也教授、山口大学大学院医学系研究科病態制御内科学講座の谷澤幸生教授らの研究グループによるもの。研究成果は、米国糖尿病学会誌「Diabetes Care」に掲載された。
糖尿病は、膵臓のβ細胞に由来するインスリンの不足や作用低下による慢性的な高血糖に特徴付けられる症候群だ。一方、膵臓部分切除術は、膵癌を含む腫瘍病変に対して施行されるが、腫瘍の発生部位により、手術術式は「膵頭十二指腸切除術」(PD)と「膵体尾部切除術」(DP)に大別される。
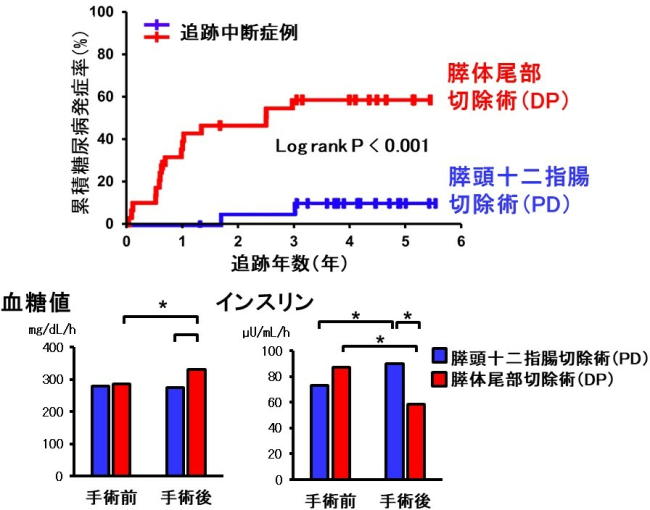
研究グループは、膵臓部分切除術前後の詳細な耐糖能の経時変化の解析により、いずれの術式も膵臓を半分程度切除するにもかかわらず、PDではDPと比較して術後5年間の糖尿病の累積発症率が著しく低い値であることを見出した。
PDでは、近位小腸のバイパス手術により術後6ヵ月の腸内細菌叢の様相が著しく変化し、糞便中の短鎖脂肪酸と小腸のL細胞に由来するインクレチンGLP-1分泌の増加にともなってインスリン分泌が増加し、糖尿病発症に抑制的に作用することが示唆された。
一方、DPでは、術後5年間に約60%が糖尿病を発症するが、切除膵臓の病理組織学的解析により、細胞の可塑性のマーカーであるALDH1A3の発現増加をともなう膵島の腫大(膵臓β細胞面積の増大)が糖尿病発症に関連することが明らかになった。
今回の研究により、術式により膵臓部分切除術後の糖尿病発症が異なることが明らかとなり、膵臓部分切除術後の糖尿病の発症予測とともに、糖尿病発症での腸内環境と膵内分泌細胞の可塑性の病態生理的意義が臨床的に証明された。
研究成果は、膵臓部分切除術後のみならず、通常の2型糖尿病の発症メカニズムの理解にも新しい洞察をもたらすものだ。
「本研究は、内科医と外科医の緊密な連携による膵臓部分切除術前後の詳細な耐糖能の解析により完成しました。臨床検体の解析にこだわり、若手の病棟担当医と大学院生が根気強く頑張ってくれて、学部を越えた多施設共同研究により臨床的に重要なメッセージを発信することができました」と、研究者は述べている。
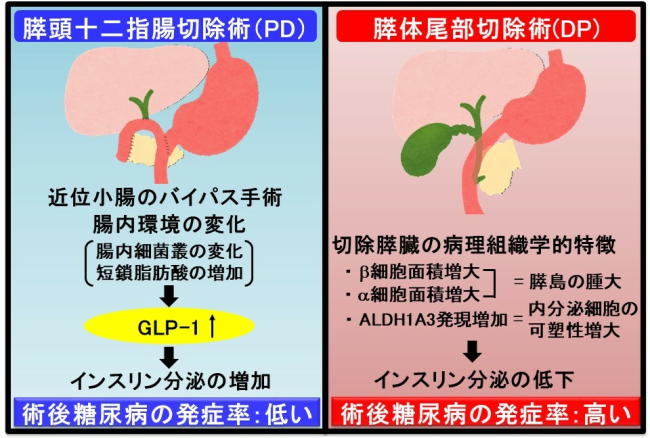
(右) 膵体尾部切除術(DP)では、切除膵臓において内分泌細胞の可塑性増大を伴う膵島の腫大がある場合、インスリン分泌が低下して術後糖尿病の発症率が高くなる。
PDを受けた患者では術後にインスリン分泌が増加 腸内細菌叢が変化しGLP-1の分泌が増加
膵臓は生体での血糖降下作用を有する唯一のホルモンであるインスリンを分泌する内分泌器官であるため、膵臓部分切除術後には糖尿病を発症する可能性が高くなる。
膵臓部分切除術の術式は、膵臓の右側半分(膵頭部と膵体部の一部)と十二指腸を切除して近位小腸をバイパスする「膵頭十二指腸切除術」(PD)と、膵体部の一部と膵尾部を切除する「膵体尾部切除術」(DP)に大別されるが、術式による術後糖尿病の発症率に差があるか否かについては複数の報告があり、一貫した結論が得られていなかった。
その要因として、過去の多くの研究で、膵臓手術の原因疾患として慢性膵炎や膵臓癌が多く含まれていたことが挙げられる。慢性膵炎や膵臓癌は疾患自体が耐糖能に影響すること、これらの疾患は死亡率が高いため長期の追跡が困難であることより、術式自体が術後糖尿病の発症にどの程度影響するのかは明らかではなかった。
そこで研究グループは、2型糖尿病を発症しておらず、慢性膵炎や膵臓癌ではない患者を対象に調査した。PDを受けた患者は、DPを受けた患者より術後糖尿病の発症率が著しく低いことを見出した。また、2つの術式では膵臓切除量が同程度であるにもかかわらず、PDを受けた患者では術後にインスリン分泌が増加していることが明らかになった。
次にPDではどのような要因が術後耐糖能に影響するのかを検討した。その結果、PDを受けた患者の腸内では術後に腸内細菌叢に著しい変化を生じること、短鎖脂肪酸の一つである酪酸の濃度とともに腸管内分泌ホルモンであるGLP-1の分泌が増加することを発見した。
糞便中の酪酸とGLP-1の分泌には正の相関関係が認められ、PDを受けた患者でのGLP-1分泌の増加は腸内の酪酸の増加による可能性が示唆された。
一方、DPを受けた患者では、膵島のインスリンを分泌するβ細胞あるいはグルカゴンを分泌するα細胞の膵臓に占める面積が大きい患者が術後に糖尿病を発症しやすいことを見出した。
さらに、β細胞やα細胞の膵臓に占める面積と膵臓内分泌細胞の可塑性のマーカーであるアルデヒド脱水素酵素1A3(ALDH1A3)の発現に正の相関関係があることを発見した。
2型糖尿病の発症メカニズムの理解に新しい洞察
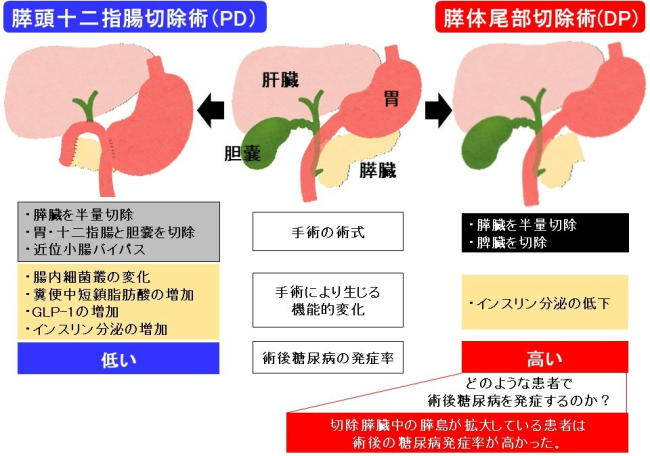
今回の研究は、膵臓部分切除術の術式により術後糖尿病の発症率に著しい差があること、近位小腸バイパス手術による腸内環境の変化あるいは切除した膵臓の病理組織学的特徴と術後糖尿病の発症の関連を明らかにしました。
これらの研究成果は、膵臓部分切除術の術後糖尿病の発症予測に有用であるともに、通常の2型糖尿病の発症メカニズムの理解に新しい洞察をもたらすものだとしている。今後、腸内環境や膵内分泌細胞の可塑性を標的とした新たな糖尿病治療法の開発が期待される。
九州大学大学院医学研究院 病態制御内科学(第三内科)
国立国際医療研究センター研究所 糖尿病情報センター
東京医科歯科大学大学院医歯学総合研究科 分子内分泌代謝学分野(糖尿病・内分泌・代謝内科)
山口大学大学院医学系研究科病態制御内科学(第三内科)
Importance of Intestinal Environment and Cellular Plasticity of Islets in the Development of Postpancreatectomy Diabetes(Diabetes Care 2021年2月24日)