老化細胞を選択的に除去する「GLS1阻害剤」 糖尿病・動脈硬化症・NASHの症状を改善 新たな抗加齢療法を開発 東大医科学研究所
2021.01.19
東京大学医科学研究所の研究グループは、加齢関連疾患の原因となる老化細胞だけを除去する「GLS1阻害剤」が、老齢マウスや加齢関連疾患モデルマウスへの投与により、さまざまな臓器・組織の加齢現象や、老年病、生活習慣病を改善できることを発見したと発表した。
老化細胞の代謝特異性を標的とした、老化細胞の除去による新たな抗加齢療法を開発できる可能性がある。
老化細胞の代謝特異性を標的とした、老化細胞の除去による新たな抗加齢療法を開発できる可能性がある。

GLS1阻害剤が肥満性糖尿病、動脈硬化症、非アルコール性脂肪肝(NASH)の症状を改善
細胞はさまざまなストレスを受けると、不可逆的な増殖停止を示す老化細胞に誘導されることが知られている。これまでに、老化細胞は加齢にともない生体内に蓄積することや、老齢マウスから遺伝子工学的に老化細胞を除去すると、動脈硬化や腎障害などの老年病の発症が有意に遅れ、健康寿命も延伸することが示されていた。 しかし、組織・臓器により老化細胞は多様性を有することが分かっており、多様な老化細胞を除去するための薬剤の開発やその標的の同定には至っていなかった。 そこで、東京大学医科学研究所の研究グループは、新たな老化細胞の純培養法を構築し、老化細胞の生存に必須な遺伝子群をスクリーニングにより探索した結果、グルタミン代謝酵素「GLS1」を同定するのに成功した。 「GLS1」の発現解析により、老化細胞はリソソーム膜に損傷が生じ、細胞内pHが低下することで、「GLS1」の阻害に対する感受性が亢進することも明らかにした。さらに老齢マウスに「GLS1阻害剤」を投与すると、さまざまな組織・臓器における老化細胞が除去され、加齢現象が有意に改善することを確かめた。 加えて、さまざまな加齢関連疾患モデルマウスに対する「GLS1阻害剤」の効果を検討した結果、肥満性糖尿病、動脈硬化症、および非アルコール性脂肪肝(NASH)の症状改善に有効であることも見いだした。 今回の研究成果により、老化細胞の代謝特異性やそれに起因する脆弱性が明らかとなり、それらを標的とする薬剤を開発することで健康寿命の亢進のみならず「がん」や「動脈硬化」などのさまざまな老年病の予防・治療への展開も期待されるとしている。 研究は、東京大学医科学研究所の城村由和助教(癌防御シグナル分野)、中西真教授(癌防御シグナル分野)らの研究グループによるもの。研究成果は、米国際科学誌「Science」に掲載された。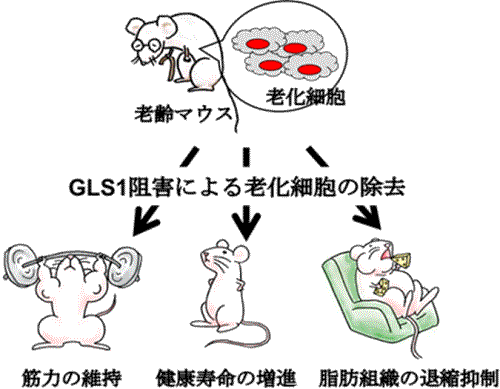
出典:東京大学医科学研究所、2021年
グルタミン代謝に関与するGLS1を有力遺伝子として同定
これまでの研究で、遺伝子工学的実験手法により、マウス個体から老化細胞を除去することで加齢にともなうさまざまな症状の改善や健康寿命の亢進、さらには動脈硬化症などの加齢関連疾患の病態が改善することが報告されてきた。 しかし最近になり、生体内に存在する老化細胞は多様性を有することが分かってきて、広範な老化細胞を標的とした老化細胞除去薬の開発には至っていない現状がある。 研究グループは公開、老化細胞の生存に必須な遺伝子群を探索するために、これまでの研究成果をもとに新たな純化老化細胞の作製法を構築した。この新しい作製法は、p53遺伝子をG2期で活性化させるもので、非常に効率的に細胞老化が誘導でき、他の誘導系で作製した老化細胞と同じ性質をもっている。 この純化老化細胞を用いて、レンチウイルスshRNAライブラリースクリーニングにより、老化細胞の生存に必須な遺伝子群の探索を行った。このスクリーニング法は、細胞内に存在するさまざまなmRNAに対応するshRNAを合成し、それらをレンチウイルスベクターを用いて細胞に導入することで、各々のmRNAから合成されるタンパク質の発現を抑制することで、個々のタンパク質の機能を網羅的に調べる方法だ。 その結果、グルタミン代謝に関与するGLS1が有力な候補遺伝子として同定された。そこで、老化細胞におけるGLS1の発現変化を解析したところ、細胞の種類や老化誘導要因にかかわらず、老化細胞においてGLS1アイソフォームの1つであるKGAの発現が顕著に増加していることが分かった。 KGAはGLS1のアイソフォームの1つで、腎臓尿細管の上皮細胞に発現することが知られている。 また、ヒトの皮膚でも、KGAの発現と年齢に正の相関があることも判明した。さらに正常細胞、および老化細胞の生存に対する「GLS1阻害剤」の影響を検討したところ、老化細胞を選択的に死滅させることが確認された。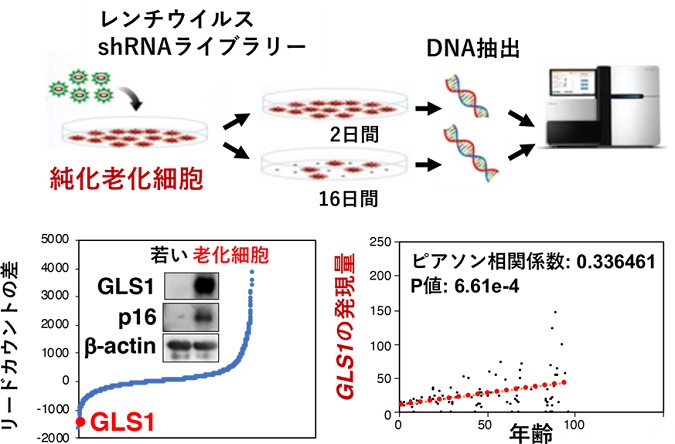
出典:東京大学医科学研究所、2021年
老化細胞でGLS1を阻害すると細胞死が誘導される
これまでのラット腎臓を用いた報告では、KGAの発現は細胞内pHの低下により発現が上昇することが示されていた。 細胞内のpHの調節にはリソソームと呼ばれる細胞内小器官が重要な役割を果たすことから、リソソームの動態について解析を行い、老化細胞でリソソーム膜に損傷が生じること、その原因が老化細胞のさまざまな遺伝子の過剰発現によるタンパク質凝集体の形成であることを明らかになった。 興味深いことに、老化細胞でGLS1を阻害すると、細胞内pHが大きく低下することで細胞死が誘導されること、そして細胞培養液のpHを弱塩基性にすることやアンモニアを過剰添加することで、GLS1阻害による細胞死が抑制されることも分かった。 GLS1は、グルタミンをグルタミン酸へと変換すると、エネルギー代謝に重要な代謝産物とともにアンモニアを産生することは以前から知られていたが、アンモニアの産生はあくまで副産物であると考えられており、その生理・病理的意義については不明だった。 今回の研究で解明された分子メカニズムにより、老化細胞は、細胞内pHの低下にともない、GLS1の量を増加することで過剰なアンモニアを生成し、細胞内pHの恒常性を調節することで生存を維持できることが示唆された。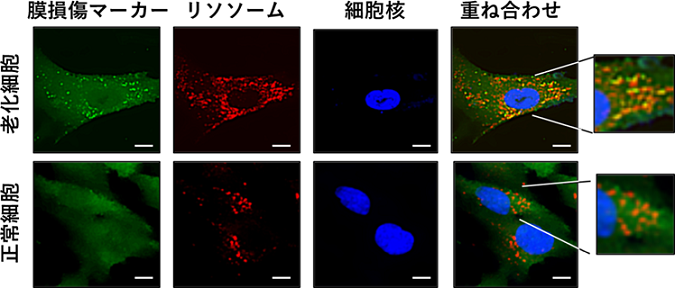
出典:東京大学医科学研究所、2021年
GLS1阻害剤は有効ながん治療薬として臨床試験中
最後に、加齢現象に対する「GLS1阻害剤」の有効性を検証するために、老齢マウスに「GLS1阻害剤」を投与したところ、さまざまな臓器・組織で老化細胞の除去が確認でき、加齢性変化の特徴として知られている「腎臓の糸球体硬化」「肺の線維化」「肝臓の炎症細胞浸潤」といったさまざまな症状が改善することが可能であることが分かった。 また、老化にともなう筋量低下による運動能力低下や脂肪組織萎縮による代謝異常を生じることが知られているが、「GLS1阻害剤」の投与により、これらの進行も抑制された。さらに、さまざまな加齢関連疾患モデルマウスへ「GLS1阻害剤」を投与したところ、肥満性糖尿病、動脈硬化、およびNASHの症状が緩和されることも分かった。 今回の研究の成果により、リソソーム膜損傷によるグルタミン代謝の亢進が老化細胞の脆弱性の分子基盤であることが明らかになった。さらに「GLS1阻害剤」が生体内での老化細胞の除去に有効であること、その結果として、さまざまな加齢現象や老年病、生活習慣病の改善に有効であることが示された。 「現在、GLS1阻害剤は有効ながん治療薬として臨床試験中であり、本研究を足がかりとして、GLS1阻害剤を用いた老化細胞除去による革新的な抗加齢療法や、「がん」を含めた老年病や生活習慣病の予防・治療薬の開発にもつながることが期待されます」と、研究者は述べている。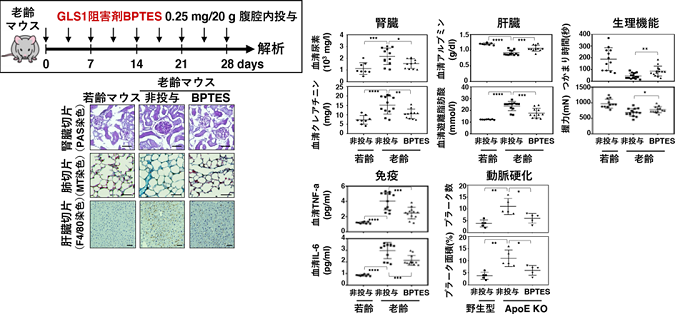
GLS1阻害剤を老齢マウスへと投与した結果、非投与群に比べて、投与群で、加齢にともない生じる腎の糸球体硬化(左上段)、肺の線維化(左中段)、および肝臓の炎症細胞浸潤(左下段)や、さまざまな臓器・生理機能が改善された(中)。また生活習慣病である動脈硬化も顕著に改善した(右)。
出典:東京大学医科学研究所、2021年
東京大学医科学研究所Senolysis by glutaminolysis inhibition ameliorates various age-associated disorders(Science 2021年1月15 日)
[Terahata / 日本医療・健康情報研究所]