【新型コロナ】COVID-19は短期間の変異で感染力がアップ 現在流行中のD614Gウイルスは感染効率がより高い 東大医科学研究所
2020.11.19
東京大学医科学研究所は、現在世界中に蔓延している新型コロナウイルス(SARS-CoV-2)のSpikeタンパク質にD614Gの変異をもつ、variantウイルスの性状解析を行い、D614G変異が、ウイルスの増殖適応と動物間の感染伝播の高さに寄与することを明らかにしたと発表した。
D614Gウイルスは、細胞への取込みが野生型ウイルスに比べて有意に速く、また、野生型ウイルスと競合培養継代し3代のうちに優勢になり、高い増殖適応性を示すようになった。
D614Gウイルスは、細胞への取込みが野生型ウイルスに比べて有意に速く、また、野生型ウイルスと競合培養継代し3代のうちに優勢になり、高い増殖適応性を示すようになった。
現在流行中のD614Gウイルスは増殖適応が高い
研究は、東京大学医科学研究所感染・免疫部門ウイルス感染分野の河岡義裕教授らの研究グループが、国立感染症研究所、ノースカロライナ大学、ウィスコンシン大学の研究グループと共同で行ったもの。研究成果は「Science」オンライン版に掲載された。 新型コロナウイルス(SARS-CoV-2)の世界的な感染拡大が続いている。その間に、Spikeタンパク質のアミノ酸残基614番のアスパラギン酸がグリシンに置換わる変異(D614G)をもつvariantウイルスが出現し、圧倒的に優勢になった。現在世界で蔓延しているのはこのvariantウイルスだ。 Spikeタンパクは、SARS-CoV-2のウイルス粒子表面に発現するタンパク質。このSpikeタンパクが宿主細胞に発現する受容体タンパクと結合することが、感染成立に必要な第一歩となる。 現在開発のすすめられているワクチンのほとんどは、このSpikeタンパクを標的として、その機能を失わせる(中和する)ことを目的としてしている。感染から回復した患者の多くで、Spikeタンパクに対する中和抗体が検出される。 D614Gは、Spikeタンパクの614番目のアミノ酸残基がアスパラギン酸(D)からグリシン(G)に置き換わる変異。このアミノ酸置換によりSpikeタンパクは、宿主受容体と結合しやすい立体構造をとる傾向が強まるため、結果としてウイルスの宿主細胞への侵入を容易にさせると考えられる。継代3代でD614Gウイルスが圧倒的に優位に
Spikeタンパク質はSARS-CoV-2のウイルス粒子表面に発現し、宿主の受容体と結合することで感染が成立する。先行研究では、タンパク質の構造解析から、Spikeタンパク質にD614Gの変異が入ることで、Spikeタンパク質が宿主の受容体に結合しやすい構造になる傾向があることが明らかにされている。しかしこれまで、D614G変異がSARS-CoV-2ウイルスの性状、増殖特性や病原性にどのような影響を与えるかという点は、細胞レベルでも感染動物個体でもよく分かっていなかった。 今回の研究ではまず、リバースジェネティクス法により、野生型ウイルスと、Spikeタンパク質D614G変異のみの違いをもつウイルス(D614Gウイルス)を人工合成した。これにより、この変異が与える影響を厳密に調べることが可能になった。 次に、野生型/D614Gそれぞれについて、感染成立のマーカーとしてルシフェラーゼを発現するウイルスを人工合成し、細胞への取り込みを比較したところ、D614Gウイルスを感染させた細胞では、感染後8時間の時点で3~8倍高いルシフェラーゼの発現が見られた。このことは、D614G変異が細胞への侵入の効率を高めていることを示す。 また、ヒト呼吸器での増殖を比較するため、ヒトの鼻上皮、肺から分離されたプライマリ細胞での増殖を比較したところ、特に鼻上皮細胞で、D614Gウイルスが有意に高い増殖を示した。これは、Vero-E6細胞やA549-ACE2細胞(ヒト肺由来細胞株A549にSARS-CoV-2の受容体であるACE-2を発現させた細胞)といった実験細胞株ではみられない傾向だった。 ウイルスの増殖適応にD614G変異が与える影響を調べるために、野生型とD614Gウイルスを1:1の割合で混合して、細胞で競合継代したところ、継代3代以内に、混合ウイルスのpopulationではD614Gウイルスが圧倒的に優位になり、野生型ウイルスはほとんど検出されなくなった。野生型とD614Gを10:1の割合で混合した場合にも、継代3代でD614Gウイルスが圧倒的に優位になった。このことは、D614G変異がウイルスの増殖適応を強めたことを示唆している。野生型ウイルスで開発されたワクチンは、D614Gウイルスでも効果が期待できる
Spikeタンパク質は、ウイルスの表面に発現することから、ワクチンのターゲットとしても重要で、D614G変異が異なる抗原性を示すか否かは、重要な問題だ。ヒト回復患者の血清を用いて、野生型、D614Gウイルスに対する中和能を比較したところ、有意な差はみられなかった。また、SARS-CoV-2のSpike-RBD(レセプター結合ドメイン)に結合するモノクローナル抗体との反応性にも、野生型、D614Gウイルス間で有意な違いがみられなかった。 このことは、D614Gが野生型ウイルスと類似した抗原性を示すことを示唆する。すなわち、野生型ウイルスをもとにして開発が進められてきたワクチンは、D614Gウイルスに対しても、野生型ウイルスに対しても同様の効果が期待されると考えられるという。 さらに、動物個体におけるD614G変異の影響を調べるために、ヒトACE2トランスジェニックマウスとハムスターを用いて感染実験を行った。まず、呼吸器でのウイルスの増殖を比較するために、同じ感染力価の野生型あるいはD614Gウイルスで感染させ、肺、鼻甲介でのウイルスの増殖を比較したところ、ヒトACE2トランスジェニックマウスとハムスターいずれでも、野生型とD614Gウイルス間で、有意な差はみられなかった。また、感染後の肺の炎症の程度にも、野生型とD614Gウイルス感染個体間で有意な差はみられなかった。すなわち、D614G変異は動物個体における病原性には大きく影響しないことがわかった。D614Gウイルスの飛沫感染効率はより高い
さらに、D614G変異がウイルスの感染伝播に与える影響を調べるため、ハムスターを用いた飛沫感染伝播実験を実施。ハムスターを、野生型ウイルスあるいはD614Gウイルスで感染させ(感染個体)、感染個体のケージから、直接接触を避けるために5cm離したケージで、非感染個体(曝露個体)を飼育した。このような、感染個体・曝露個体のペアを、野生型、D614Gウイルスそれぞれについて8ペア用意した。 野生型ウイルスについては、2日後では曝露個体の鼻洗浄液からウイルスは検出されなかったが、4日後には8ペアの曝露個体全てからウイルスが検出された。一方、D614Gウイルスでは、曝露から2日後の時点で8ペア中5ペアの曝露個体でウイルスが検出された。この結果は、D614G変異がより高い飛沫感染効率に寄与していることを示唆する。D614Gウイルスは非常に短期間で元の野生型ウイルスを凌駕
最後に、ウイルスの増殖適応を動物個体で比較するために、ハムスターで競合継代実験を行った。ハムスターを野生型:D614G=1:1の混合ウイルスで感染させ、3日後に肺から分離されたウイルスで、次代のハムスターを感染させた。3代の継代で、肺から分離されるウイルスのpopulationはD614Gウイルスが優位になった。 この結果は、細胞株のみならず、動物個体でもD614G変異が増殖適応性を強めていることを示唆する。研究グループは、今回の結果について、「D614Gウイルスが非常に短期間で元の野生型ウイルスを凌駕して感染拡大したことを説明付けるものと考えられる」と、述べている。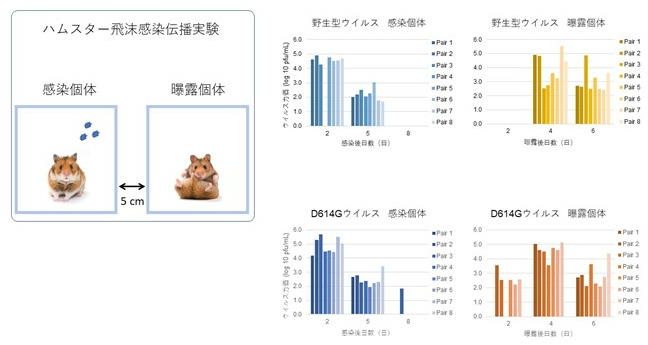
出典:東京大学医科学研究所、2020年
東京大学医科学研究所SARS-CoV-2 D614G Variant Exhibits Efficient Replication ex vivo and Transmission in vivo(Science 2020年11月12日)
[Terahata / 日本医療・健康情報研究所]











