糖尿病網膜症での「網膜機能障害」を解明 神経栄養因子「BDNF」の減少が関与 EPA内服で発現が改善
2020.02.19
名古屋大学の研究グループは、糖尿病網膜症における「網膜機能障害」のメカニズムを解明し、網膜障害を抑制するメカニズムとその効果を明らかにしたと発表した。
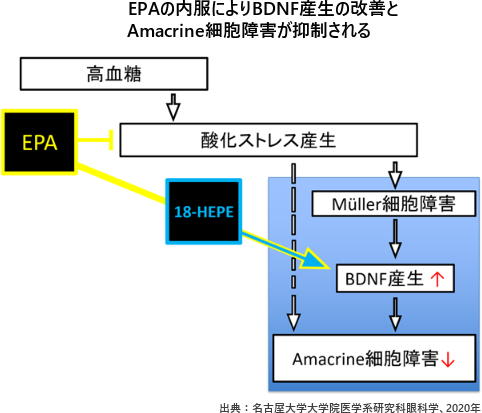
網膜機能障害にはMüller細胞から産生される神経栄養因子「BDNF」の減少が関与しており、エイコサペンタエン酸(EPA)の内服で網膜内BDNFの発現が改善することを確かめた。
網膜機能障害にはMüller細胞から産生される神経栄養因子「BDNF」の減少が関与しており、エイコサペンタエン酸(EPA)の内服で網膜内BDNFの発現が改善することを確かめた。
糖尿病網膜症の早期からの神経保護治療が重要
研究は、名古屋大学大学院医学系研究科眼科学の鈴村文那氏、兼子裕規氏、寺﨑浩子教授らの研究グループによるもの。研究成果は「Diabetes」に掲載された。 糖尿病網膜症(DR)では、不可逆的な「網膜機能障害」(網膜内神経細胞の障害)が問題となるため、早期からの神経保護治療が重要だが、診断基準となる眼底異常の所見が出現する前から障害は起きているとされている。 網膜機能障害が起こると、入ってきた光を電気エネルギーに変換して脳へと情報を送るという網膜の機能が正常に働かなくなる。 DRは初期の段階から、「Neurovascular unit」の障害として、神経変性と微小血管の障害が密接に関わっており、網膜内神経細胞がDRに大きく影響する新たな血管形成に関与していることが知られている。 研究グループは、神経細胞の成長、維持や再生を促進するタンパク質である「BDNF」に着目。神経栄養因子の中でもBDNFは糖尿病で低下するとされている。 今回の研究では、ω3脂肪酸の1つであるエイコサペンタエン酸(EPA)を内服することにより、視床下部でのBDNF産生が改善されるという報告をもとに、EPA内服による眼内でのBDNF産生の改善と網膜機能改善の可能性を検討した。 これまでもBDNFの硝子体注射やBDNFを産生する遺伝子組み換え細胞の網膜下移植などの方法が試みられてきたが、いずれも侵襲性は低くはなかった。 EPA内服というより低侵襲な方法により、眼内でのBDNF産生と網膜機能を改善できる可能性がある。EPA内服で網膜内BDNFの発現が改善
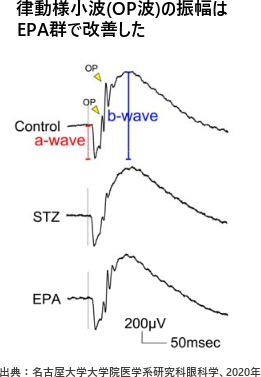
具体的には、DR患者の硝子体中の活性酸素濃度が明らかに高いことと、DR発症に酸化ストレスが関与していることから、細胞実験を行い、酸化ストレスとして過酸化水素を細胞に投与することでDRモデルとした。 「Müller細胞」は、網膜を構成する細胞の一種で、網膜内の他の細胞機能維持にも関与している。 研究グループは、BDNFを産生するMüller細胞としてMIO-M1細胞を網膜内神経細胞であるAmacrine細胞としてPC12D細胞を用い、それぞれに対して過酸化水素を投与した。 その結果、それぞれの細胞増殖の機能は低下し、MIO-M1細胞のBDNF産生機能も低下した。 一方、PC12D細胞に対してBDNFを投与したところ、その軸索の長さが短くなる変化が抑えられ、酸化ストレス下のPC12D細胞でも投与するBDNFの濃度が高いほど、細胞増殖の機能は改善した。 次に、動物実験ではストレプトゾシン(STZ)という薬剤をラットの腹腔内に注射して糖尿病モデルラットとした。これをコントロール群・STZ群・EPA群の3グループに分け、EPA群には5%EPAを含む餌を与え、コントロール群とSTZ群に対してはω3脂肪酸を含まず、かつ5%ひまわり油を含む餌を与えた。 8週間これらの餌をそれぞれ与えた後、全身状態の評価と、網膜に強い光を当てて発生した電位の変化を記録する「網膜電図」、網脈絡膜サンプルの解析を行った。 実験開始から8週間後、STZ群とEPA群では、コントロール群と比較して体重の減少・血糖値が上昇し、ケトーシスにもなっていたが、これら2群間には明らかな差はなかった。 一方、網膜電図にてAmacrine細胞由来とされる律動様小波(OP波)をそれぞれ比較したところ、STZ群で低くなっていたOP波の振幅はEPA群で明らかに改善していた。 また、網脈絡膜サンプルの解析により、STZ群で上昇した酸化ストレスマーカーはEPA群で低下し、STZ群で低下したBDNF産生量はEPA群で明らかに改善した。18-HEPEがBDNF産生・網膜内神経細胞機能を改善
Omega-3 Fatty Acid and its Metabolite 18-HEPE Ameliorate Retinal Neuronal Cell Dysfunction by Enhancing Müller BDNF in Diabetic Retinopathy(Diabetes 2020年2月6日)
[Terahata / 日本医療・健康情報研究所]














