敗血症性AKIにおける急性腎障害マーカー L-FABPの可能性
第45回 日本集中治療医学会 学術集会 教育セミナー23より
敗血症は急性腎障害(AKI)を併発することが多く、AKIを発症すると予後はさらに深刻となる。予後改善に向けより早期からの介入が必要だが、AKI診断のクライテリアである血清クレアチニン上昇や尿量低下は腎障害の結果として生ずる変化であるため、それだけでは介入の遅れを免れない。これに対し、新たなバイオマーカーが早期診断の一助となる可能性が示されつつある。
その最前線の研究から見えてきた敗血症性AKIの新たなパラダイムを、湘南鎌倉総合病院集中治療部医長の小室哲也先生に講演いただいた。

演者:小室 哲也 先生
(医療法人沖縄徳洲会 湘南鎌倉総合病院 麻酔科・集中治療部。現在:自治医科大学附属さいたま医療センター 集中治療部)

司会:野入 英世 先生
(東京大学医学部附属病院 腎臓・内分泌内科)
Prologue AKIの見つけ方
東京大学医学部附属病院 腎臓・内分泌内科 野入 英世 先生
本講演では湘南鎌倉総合病院の小室先生をお迎えし敗血症性AKIの診断と治療について講演いただくが、その前に私からプロローグとして「AKI の見つけ方」を少しお話ししたい。
AKIを早期診断できていない
図1は、AKIが発生しGFRが90mL/分/1.73m2から10mL/分/1.73m2へ一気に低下した際、血清クレアチニンがどのように変化するかをシミュレーションしたものだ。24時間経過した時点で血清クレアチニンは2mg/dL、48時間で4、それぞれの時点のeGFRは38、18mL/分/1.73m2となる。そして7日後にようやく血清クレアチニン7、eGFR 10に至る。本来は直ちにGFRが10に落ちたことがわからなければいけないにもかかわらず、これだけのタイムラグがあるということだ。血清クレアチニンは腎機能評価のゴールドスタンダードではあるが、それだけでは介入のタイミングを失しかねない。
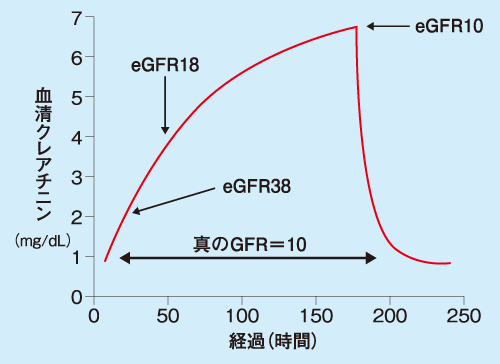
〔J Am Soc Nephrol 20:672-679,2009〕
早期診断はICUではノイズにもなり得る
この問題に対応し、これまでにL-FABP(liver-type fatty acid-binding protein)やNGAL(neutrophil gelatinase-associated lipocalin)などさまざまなバイオマーカーが開発されてきた。しかし、ERにおける各種バイオマーカーのAKI診断能を比較した報告などから、いずれのマーカーも陰性的中率が非常に高い反面、陽性的中率がやや低いことが知られている1)。もちろん、バイオマーカーでAKIを否定できるということは、ERでは一つの利点となるだろう。しかしICUでは何らかの手段で陽性的中率も高めなければ治療に結び付けづらい。つまり、高い感度を保ちながらも、介入せずとも回復していくようなノイズを入り込ませない重症度判定が理想とされる。具体的には、ICUにおいてKDIGOのステージ1ではノイズが多く介入すべきポイントはさほど多くないことから、KDIGOステージ2以上が抽出すべき対象ではなかろうか。
RAIを用いてpersistent AKIを診断
こうした中、AKIが3日以上続き積極的な介入が必要となる可能性が高いと予測されるAKIの新たな定義として'persistent AKI'という概念が打ち出され、徐々に定着してきている2)。そのpersistent AKIの抽出法として、血清クレアチニンやGFRの変動幅に種々の患者背景をスコア化し乗算して算出する'Renal Angina Index('RAI)という指標が既に存在し、さらに的中率を高めるべく改良した計算式も複数提唱されている。我々もRAIの計算式にL-FABPを上乗せすることで、persistent AKIの診断能が有意に上昇することを報告している(図2)。このような手法によりpersistent AKIを早期に効率的に見出すことで、今後AKIの予後改善に向けた検討が可能になっていくだろう。
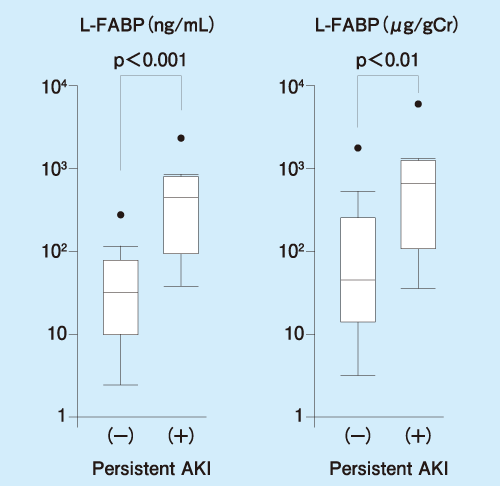
〔Kidney Int Rep(in press)〕
敗血症性AKIにおける急性腎障害マーカーL-FABPの可能性
医療法人沖縄徳洲会 湘南鎌倉総合病院 麻酔科・集中治療部
(現在:自治医科大学附属さいたま医療センター 集中治療部) 小室 哲也 先生
AKIの診断基準は過去からRIFLE、AKIN、KDIGOと進化してきた。しかしそれらのいずれも血清クレアチニンと尿量から診断するもので、この十年、診断基準の構成要素に大きな変化はみられない。そして現在もICUにおけるAKI発症の寄与死亡率は8.6%に上ると報告されており3)、AKIをより早く診断したいというのは恐らく、腎臓内科医、救急医、集中治療医、全ての医師に共通する想いだろう。
これに対して過去にさまざまなバイオマーカーが臨床応用されてきた。コラーゲンIVやβ2MG(β2-microglobulin)、シスタチンCなどは私が研修医のころから知られているものだ。しかし現在これらを用いて臨床判断しているという印象は乏しい。そんな中、近年、novelバイオマーカーと呼ばれるものが登場し、ガイドラインにも「早期診断に有用な可能性がある」と記されている(表1)。野入先生のお話にあったようにAKIの診断と治療は今、新しいフェーズに入ろうとしているようだ。そのような可能性を感じさせるnovelバイオマーカーの中から本日はL-FABPを取り上げる。
表1 AKI診療ガイドラインにおけるnovelバイオマーカーの位置づけ
| CQ5-1 |
|---|
| CQ5-1 AKIの早期診断として尿中バイオマーカーを用いるべきか? |
| 尿中NGAL、L-FABPはAKIの早期診断に有用な可能性があり測定することを提案する。尿中シスタチンCの有用性は限定的で明確な推奨はできない。 尿中NGAL、尿中L-FABP: 推奨の強さ 2 エビデンスの強さ B 尿中シスタチンC: 推奨の強さ なし エビデンスの強さ C |
〔AKI(急性腎障害)診療ガイドライン2016. 東京医学社,2016〕
L-FABPによる敗血症性AKIの早期診断
L-FABPは尿細管に発現する蛋白質で、虚血や酸化ストレスにより増加し尿中に排泄される。先行研究から、人工心肺を用いた心臓外科手術においてAKIを起こした群はL-FABPがポンプ離脱後4時間という早期から有意に上昇することや4)、造影剤腎症の発症を予測可能といった5)、有用性に関する報告が増えている。
では、敗血症ではどうだろう。敗血症にAKIを合併すると、それぞれ単独の発症に比べて死亡率が有意に上昇することが知られている6)。このような敗血症性AKIの診断にL-FABPは有効だろうか。
当院で行った「SHOCK-SEPSIS study」(shonan observation cohort for acute kidney injury with sepsis study)の結果を紹介する。対象は2017年の5~10月に敗血症によりICU管理を要した95例。ICU入室後3日以内に採取した尿を用いてL-FABPを測定し、28日間追跡した。主な患者背景は、年齢78歳、男性72%、SOFAスコア7、敗血症性ショック43名(45%)、尿量1,230mL/日など。このうち58例が追跡期間中にKDIGOステージ1以上のAKIと診断された。AKI発症群と非発症群のL-FABPを比較すると、前者が有意に高値であり(p=0.0008)、L-FABPがAKIの早期診断に有用であることが確認された。
なお、この検討ではL-FABPの定量検査のほかにPOCキット(シミックホールディングス製)を用いた。このキットは必要検体量がごくわずかであり、結果も半定量ながらごく短時間でわかる。精度に関しても今回の検討で、判定が陰性の群と陽性の群とでL-FABPの実測定量値に有意差があり、一定の信頼性が認められた。特にKDIGOステージ2以上の診断において、判定がマイナスの場合の陰性的中率が87%と高い値を示し、AKIの否定に有用と考えられた。定量値との乖離が散見されることや尿pHの影響を受けるなどの改善点もあるようだが、ICUなどの限られた時間で臨床判断が迫られる状況において実用的である。
バイオマーカーの併用による敗血症性AKIの病態把握・治療介入の試み
では、このようなL-FABPをはじめとするバイオマーカーの敗血症性AKI診療における活用法を考えてみたい。
敗血症によって生ずる腎障害の基盤には、ショックによる血圧低下や循環血液量減少など腎前性の因子による「虚血」と、その虚血や敗血症そのものによる腎実質の「炎症」という二つの要素がある。ここで、各種バイオマーカーの特性を主成分分析した図3をみると、L-FABPは乳酸と同じ傾きであり主に組織低灌流・虚血を反映するマーカーであることがわかる。一方、炎症を反映するマーカーとしては、CRPと同方向に傾くNGALが挙げられる。よってL-FABPとNGALの双方を用いることでAKIを早期に診断できる可能性があ る(図4)。

〔Scientific Reports 6(33077),2016〕

敗血症性AKIの病態診断の可能性
実際に、解析対象は敗血症性AKIではなく心臓外科手術後のAKIであるものの、L-FABPとNGALの両者を測定しAKI発症を予測する研究が中国で行われた7)。それによると、両者の併用によりAKI診断のROC曲線下面積が0.9以上という極めて高い値に上り、先ほど野入先生がおっしゃったKDIGOステージ2以上のAKIの診断精度の上昇も期待できる結果が報告されている。
さて、これらの知見をもとに、敗血症性AKIにおけるバイオマーカーの活用法を探ってみたい。図5のように、虚血のマーカーとしてL-FABPを横軸にとり、炎症のマーカーとしてNGALを縦軸にとって、全体を四つのクラスターに分けて考える。L-FABPとNGALの双方が高い群がクラスター①で、炎症と虚血が関与している重症例ということだ。十数例とわずかではあるが自験例をこれに当てはめてみたところ、クラスター①は敗血症ショック症例、④はAKI非発症例が多く占めることが確認できた。

敗血症性AKIクラスター分類(私案)
ここまでの診断プロセスのチャートを図6に示す。ICUにおいては時間が優先されることからL-FABPについてはとりあえずPOCキットの結果をもとにクラスターを仮判定しておき、L-FABPの定量値が出たら確定とするという流れだ。ただし、このクラスター分類についてはあくまでもまだ理論的な私見で あり、適切なカットオフ値の設定も含め多くの検証が必要な段階であることをご承知いただきたい。

さらに私見を重ねることになるが、仮にこのような分類が可能であるとすると、図7のような病態に即した初期治療が可能になるかもしれない。炎症と虚血があるクラスター①は、PMX(polymyxin B-immobilized fiber)とRRT(renal replacement therapy)を併用するか否かはさておき、血液浄化がまず優先されるだろう。クラ スター②は虚血がベースなので循環管理、クラスター③は炎症ベースなのでRRTを優先的に考慮する必要がありそうだ。クラスター④は経過観察もしくはAKIとは異なる因子を考慮すべきかもしれない。

PMXの効果判定にL-FABPが有用な可能性
ところでPMXはその有効性についていまだ議論が続いているが、敗血症性AKIに対するPMXの効果をL-FABPで検討した結果が報告されている8)。それによるとPMXによらず古典的な治療を行った群ではエンドトキシンもL-FABPもわずかな低下にとどまったが、PMXを施行した群では両者ともに有意に低下したという。L-FABPは介入ポイント を探るという目的以外に、治療効果の判定にも使える可能性がありそうだ。
以上、データの裏付けが少ない話もしたが、従来の診断クライテリアにバイオマーカーを上乗せしAKIを診断することで、より早期に病態に即した治療を行うという次の時代へのパラダイムシフトは近づいているように感じている。
Discussion ―フロアとの質疑応答―
―― NGALとL-FABPの保険適用について教えてください。
野入先生 NGALはAKIに対して3回まで算定できます※。L-FABPは腎障害が疑われる時点で使えるので、AKIに限らず糖尿病性腎症のようなCKDでも使えます。CKDでは3カ月に1回算定でき、AKIではNGALに準じますが、症状詳記によりそれ以上認められることもあります。小室先生のご講演にNGALとL-FABPを併用するお話がありましたが、保険診療で算定できるのは一方のみですので、DPC病院ならともかく、そうでない場合は難しいかもしれません。
―― L-FABPの定量を外注すると何日ぐらいで帰ってくるのでしょうか?
野入先生 受託業者によるのですが、1~3日だと思います。ただしL-FABPには複数の測定系があり、院内の一般的な汎用自動分析装置で測定できる系(積水メディカル製)もあります。
※NGALの算定条件:急性腎障害の診断時又はその治療中に、CLIA法により測定した場合に算定できる。ただし、診断時においては1回、その後は急性腎障害に対する一連の治療につき3回を限度として 算定する。なお、医学的必要性からそれ以上算定する場合においては、その詳細な理由を診療報酬明細書の摘要欄に記載すること。
参考文献
初 出
第45回 日本集中治療医学会 学術集会 教育セミナー23第10会場
(幕張メッセ国際会議場 1F 105)
演題:敗血症性AKIにおける急性腎障害マーカー L-FABPの可能性
司会:東京大学医学部附属病院 腎臓・内分泌内科 野入 英世 先生
演者:医療法人沖縄徳洲会 湘南鎌倉総合病院 麻酔科・集中治療部
(現在:自治医科大学附属さいたま医療センター 集中治療部) 小室 哲也 先生
共催:積水メディカル株式会社、シミックホールディングス株式会社











