新型コロナウイルスの感染を阻止する薬剤を同定 急性膵炎治療薬「ナファモスタット」がウイルスの侵入過程を効率的に阻止 東京大学医科学研究所
2020.03.19
東京大学医科学研究所は、新型コロナウイルス感染症(COVID-19)の阻止を期待できる国内既存薬剤として、「ナファモスタット(商品名:フサン)」を同定したと発表した。
COVID-19の原因ウイルスSARS-CoV-2の感染の最初の段階であるウイルス外膜と、感染する細胞の細胞膜との融合を阻止することで、ウイルスの侵入過程を効率的に阻止できる可能性がある。
COVID-19の原因ウイルスSARS-CoV-2の感染の最初の段階であるウイルス外膜と、感染する細胞の細胞膜との融合を阻止することで、ウイルスの侵入過程を効率的に阻止できる可能性がある。

国内で実績のある薬剤で速やかに臨床治験が可能
今年3月初めにドイツのグループはナファモスタットの類似の薬剤である「カモスタット(商品名:フォイパン)」のSARS-CoV-2に対する有効性を発表したが、これに比べナファモスタットは10分の1以下の低濃度でウイルスの侵入過程を阻止できるという。 ナファモスタット、カモスタットともに急性膵炎などの治療薬剤として本邦で開発され、すでに国内で長年にわたって処方されてきた薬剤であり、安全性については十分な臨床データが蓄積されており、速やかに臨床治験を行うことが可能だとしている。 SARS-CoV-2が人体に感染するには、細胞の表面にある受容体タンパク質(ACE2受容体)に結合したのち、ウイルス外膜と細胞膜の融合を起こすことが必要となる。コロナウイルスの場合、Spikeタンパク質(Sタンパク質)がヒト細胞の細胞膜のACE2受容体に結合した後に、タンパク質分解酵素であるTMPRSS2で切断され、Sタンパク質が活性化されることが、ウイルス外膜と細胞膜との融合には重要になる。 井上教授らは、MERSコロナウイルスでの研究結果をもとに、ナファモスタットやカモスタットの作用を調べたところ、ナファモスタットは1-10 nMという低濃度で顕著にウイルス侵入過程を阻止することを発見した。ナファモスタットはSARS-CoV-2感染を極めて効果的に阻害する可能性がある。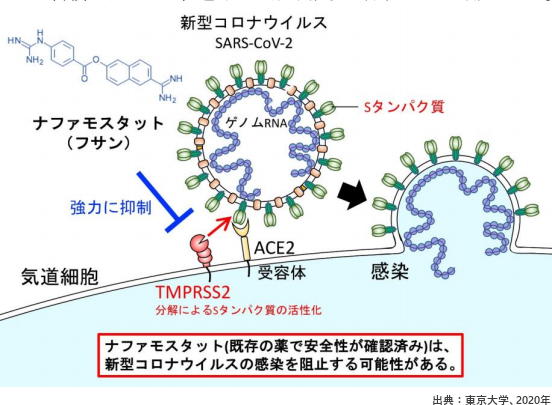
新型コロナウイルスの感染阻止を期待できる国内既存薬剤を同定
東京大学医科学研究所アジア感染症研究拠点の井上純一郎教授と山本瑞生助教は、新型コロナウイルス感染症(COVID-19)の原因ウイルスであるSARS-CoV-2が細胞に侵入する最初の過程であるウイルス外膜と細胞膜との融合を、安全かつ定量的に評価できる膜融合測定系を用いて、セリンプロテアーゼ阻害剤である「ナファモスタット」が膜融合を阻害することを見いだした。 新型コロナウイルス(SARS-CoV-2)が原因となる感染症(COVID-19)は、世界152ヵ国に拡散し、世界保健機構(WHO)も3月11日にパンデミックを宣言した。日本では、感染者の多くが無症候性キャリアもしくは軽症であるものの、重症化しさらに高齢者や基礎疾患がある人の場合には死に至ることがある。 COVID-19の治療薬の開発が急務とされており、安全性が確認された既存の薬から治療薬を探す「ドラッグリポジショニング」が有効と考えられる。 SARS-CoV-2などのコロナウイルスは、脂質二重層と外膜タンパク質からなるエンベロープ(外膜)でウイルスゲノムRNAが囲まれている。SARS-CoV-2はエンベロープに存在するSpikeタンパク質(Sタンパク質)が細胞膜の受容体(ACE2受容体)に結合したあと、ヒトの細胞への侵入を開始する。 Sタンパク質はFurinと想定されるヒト細胞由来のプロテアーゼ(タンパク質分解酵素)によりS1とS2に切断される。その後S1が受容体であるACE2受容体に結合する。 もう一方の断片S2はヒト細胞表面のセリンプロテアーゼであるTMPRSS2で切断され、その結果膜融合が進行する。SARS-CoV-2の感染にはACE2とTMPRSS2が気道細胞において必須となる。 井上教授らは、2016年にMERS-CoV Sタンパク質、受容体CD26、TMPRSS2に依存した膜融合系を用いてセリンプロテアーゼ阻害剤であるナファモスタットが膜融合を効率よく抑制してMERS-CoVの感染阻害剤になることを提唱した。 そこで今回、293FT細胞(ヒト胎児腎臓由来)を用いてSARS-CoV-2 Sタンパク質、受容体ACE2、TMPRSS2に依存した膜融合測定系を用いて、ナファモスタットがSARS-CoV-2 Sタンパク質による膜融合を抑制するかどうか検討した。 その結果、ナファモスタットは10から1000nMの濃度域で濃度依存的に抑制することが明らかになった。 さらに井上教授らはナファモスタットと類似のタンパク質分解阻害剤であるカモスタットの作用を比較検討したところ、SARSCoV-2 Sタンパク質による融合において、ナファモスタットはカモスタットのおよそ10分の1の濃度で阻害効果を示すことが明らかになった。 次にACE2やTMPRSS2を内在的に発現し、ヒトで感染が起こる際に重要な感染細胞と考えられる気道上皮細胞由来のCalu-3細胞を用いて同様の実験を行ったところ、さらに低濃度の1-10 nMで顕著に膜融合を抑制した。この濃度域はMERS-CoV Sタンパク質による膜融合に対する抑制濃度域とほぼ同じだ。 以上から、臨床的に用いられているタンパク分解阻害剤の中ではナファモスタットが最も強力であり、COVID-19に有効であると期待される。 ナファモスタット、カモスタットともに膵炎などの治療薬剤として本邦で開発され、すでに国内で長年にわたって処方されてきた薬剤だ。 ナファモスタットは臨床では点滴静注で投与されるが、投与後の血中濃度は今回の実験で得られたSARS-CoV-2 Sタンパク質の膜融合を阻害する濃度を超えることが推測され、臨床的にウイルスのヒト細胞内への侵入を抑えることが期待される。 カモスタットは経口剤であり、内服後の血中濃度はナファモスタットに劣るとみられるが、他の新型コロナウイルス薬剤と併用することで効果を期待できる。 研究は、国立研究開発法人日本医療研究開発機構(AMED)による感染症研究国際展開戦略プログラム(J-GRID)の支援を受け行われている。 東京大学医科学研究所[Terahata / 日本医療・健康情報研究所]