寄生虫が1型糖尿病の発症を抑える仕組みを解明 腸内菌が分泌する糖がT細胞を誘導 自己免疫疾患の予防・治療に新たな光
2020.11.18
理化学研究所などは、自己免疫疾患である1型糖尿病発症の抑制に関わる「CD8陽性制御性T細胞」(CD8Treg)の誘導メカニズムを発見したと発表した。
腸管寄生線虫の「H. polygyrus」に感染すると、白血球の一種でであるCD8Tregが誘導され、それにより1型糖尿病の発症が抑制されるという。
CD8Tregの誘導には、寄生虫が分泌するトレハロースと、それによって増殖した腸内細菌が必要だという。
腸管寄生線虫の「H. polygyrus」に感染すると、白血球の一種でであるCD8Tregが誘導され、それにより1型糖尿病の発症が抑制されるという。
CD8Tregの誘導には、寄生虫が分泌するトレハロースと、それによって増殖した腸内細菌が必要だという。

研究は、理化学研究所生命医科学研究センター粘膜システム研究チームの下川周子客員研究員(国立感染症研究所寄生動物部主任研究官、群馬大学大学院医学系研究科生体防御学協力研究員)と大野博司チームリーダー、国立感染症研究所寄生動物部の久枝一部長らの研究グループによるもの。研究成果は、オンライン科学雑誌「Nature Communications」に掲載された。
寄生虫を介したCD8陽性制御性T細胞の誘導により、1型糖尿病の発症が抑制される
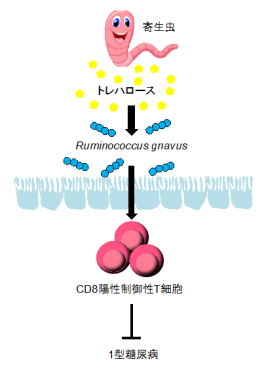 H.polygyrusによる1型糖尿病の発症抑制とCD8Tregの関係
H.polygyrusによる1型糖尿病の発症抑制とCD8Tregの関係
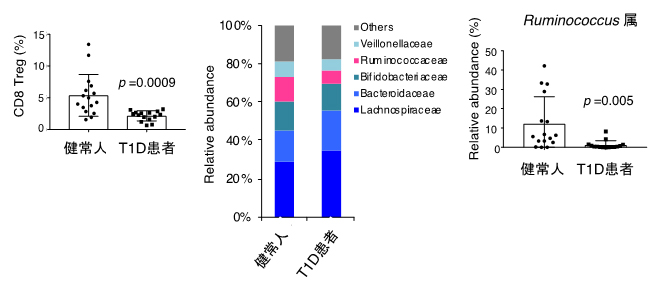
1型糖尿病( T1D)の患者における血中CD8Treg量と糞便中のRuminococcus属の腸内細菌
CD8+ regulatory T cells play a critical role in prevention of autoimmune-mediated diabetes(Nature Communications 2020年4月22日)
感染症の減少が自己免疫疾患の増加の原因?
衛生環境の改善によって、寄生虫病や結核などの感染症は減少したが、アレルギーや自己免疫疾患などの現代病は増加の一途をたどっている。とくに、寄生虫の感染者数が劇的に減少した地域では、自己免疫疾患の患者数が増加しているという報告がある。このように、現代病が増加したのは、感染症が減少したためではないかという考えを「衛生仮説」と呼んでいる。 寄生虫に感染すると、宿主(ヒト、マウスなど)は免疫機能を発達させ、寄生虫を体外へ排出しようとする。これに対して、寄生虫は宿主の免疫機能を低下させるシステムをもつため、宿主の攻撃を回避できると考えられている。 したがって、寄生虫の感染症の予防・治療にはそのシステムの解明が重要であり、寄生虫が誘導する(免疫抑制性の)細胞の種類や分泌する物質を同定する研究が世界中で行われている。 一方、1型糖尿病は、膵臓ランゲルハンス島のβ細胞が、自己の免疫細胞によって破壊され発症する疾患で、世界的に発症者が増加している。自己免疫疾患は、本来は外来から侵入してくるすべての異物から生体を守るはずの免疫システムが異常をきたし、誤って自分自身の細胞や組織を攻撃してしまう疾患だ。 研究グループは、自己免疫疾患の中で、1型糖尿病をターゲットとし、寄生虫の一種である腸管寄生線虫の感染が与える影響を調べた。腸管寄生虫に感染するとT細胞が増え、1型糖尿病発症が抑制される
研究グループは、1型糖尿病のマウスモデルを、ストレプトゾトシン(STZ)を低濃度で繰り返し投与することで作製。STZは膵臓のβ細胞をとく異的に破壊するため、マウスに投与するとインスリンが産生されなくなり、高血糖が引き起こされる。 しかし、あらかじめ腸管寄生線虫である「Heligmosomoides polygyrus」(H. polygyrus)をマウスに感染させると、1型糖尿病を誘導しても血糖値の上昇が抑えられ、β細胞の破壊もみられなかった。。これにより、H. polygyrusは1型糖尿病の発症を抑制すると考えられる。 H. polygyrusは、腸管に寄生する線虫の一種で、さまざまな免疫応答を引き起こす、慢性感染のモデルとして使用されている。 次に、そのメカニズムを調べるために、H. polygyrusが感染した際の免疫応答を調べた。これまでH. polygyrusの感染で、さまざまな免疫抑制性の細胞が誘導されることが報告されているが、研究グループは、その中で「CD8陽性制御性T細胞」(CD8Treg)に着目した。 CD8Tregは白血球の一種で、炎症性疾患、腫瘍免疫、移植寛容、自己免疫疾患などに対する新たな治療戦略の糸口になると考えられている。 実際、マウスにH. polygyrusを感染させると、CD8Tregが増加し、感染マウスからその細胞を除去すると1型糖尿病を発症するのを確認。また逆に、非感染マウスにCD8Tregを移入することで、1型糖尿病の発症が抑制された。これらの結果から、H. polygyrusによる1型糖尿病発症の抑制にはCD8Tregが重要であることが明らかになった。 H.polygyrusによる1型糖尿病の発症抑制とCD8Tregの関係
H.polygyrusによる1型糖尿病の発症抑制とCD8Tregの関係

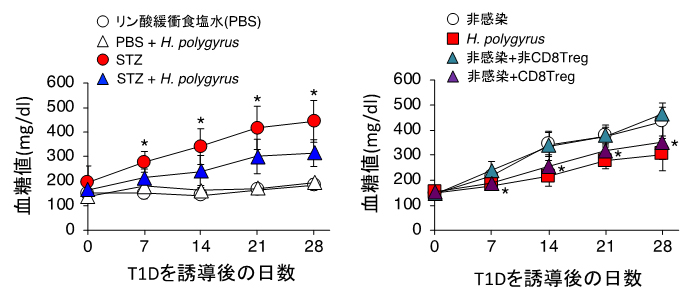
[左]STZを投与すると血糖値が上昇しT1Dを発症するが(赤丸)、あらかじめH. polygyrusを感染させたマウスにSTZを投与すると血糖値の上昇が抑えられた(青三角)。
[右]H. polygyrus感染マウスからCD8陽性制御性T細胞(CD8Treg)を単離し、非感染マウスに移入すると感染マウス(赤四角)と同様に血糖値の上昇が抑えられた(紫三角)。
[右]H. polygyrus感染マウスからCD8陽性制御性T細胞(CD8Treg)を単離し、非感染マウスに移入すると感染マウス(赤四角)と同様に血糖値の上昇が抑えられた(紫三角)。
出典:理化学研究所、2020年
寄生虫がトレハロースを分泌、腸内細菌の餌に
次に、H. polygyrusがどのようにCD8Tregを誘導するのか調べた。H. polygyrusは、主に小腸上部(十二指腸)に寄生する寄生虫だ。そこで、H. polygyrus感染マウスの小腸内容物にある代謝産物を、ガスクロマトグラフ質量分析計(GC/MS)を用いて解析した。 すると、感染マウスでは腸管内で糖の「トレハロース」が増加していること、そのトレハロースはH. polygyrus自身が分泌していることが分かった。 トレハロースは、グルコースがグリコシド結合してできた二糖の一種。食品以外に化粧品、飼料などに使用されている。また、耐糖能改善の効果、神経変性疾患抑制の効果、細胞保護の作用など、さまざまな生理機能があることが知られている。 トレハロースは腸内細菌の餌になることから、次世代シーケンサーを用いて腸内細菌叢の変化を解析したところ、H. polygyrusが感染することで、Ruminococcus属の細菌が増加していることを突き止めた。 その中でもとくにトレハロースを投与したマウスで増加した「Ruminococcus gnavus」(R. gnavus)を野生型マウスに経口投与すると、CD8Tregが誘導され、さらにSTZを投与することで1型糖尿病の発症を誘導しても血糖値の上昇が抑えられることが分かった。 この結果から、H. polygyrusによる1型糖尿病の発症抑制に関わるCD8Tregは、寄生虫が分泌するトレハロースで増殖したR. gnavusによって誘導される可能性が示された。
[左]T1D患者の血液中のCD8Tregをフローサイトメトリーで解析すると、健常人と比べて少なかった。
[中・右]T1D患者の糞便を回収し、次世代シーケンサーを用いて腸内細菌叢の解析を行うと、ピンクで示すRuminococcaceae科に含まれるRuminococcus属も少なかった。
[中・右]T1D患者の糞便を回収し、次世代シーケンサーを用いて腸内細菌叢の解析を行うと、ピンクで示すRuminococcaceae科に含まれるRuminococcus属も少なかった。
出典:理化学研究所、2020年
1型糖尿病の新たな予防・治療法の開発に向けて
CD8Tregはこれまでに、多発性硬化症や全身性エリテマトーデスなどの自己免疫疾患に効果があることが動物モデルで示されているが、その誘導メカニズムは分かっていなかった。 今回の研究で、CD8Tregの誘導には、寄生虫が分泌するトレハロースとそれによって増殖した腸内細菌が必要であることが明らかになった。 1型糖尿病には膵移植や膵島移植といった治療も選択肢の1つとして考えられるが、深刻なドナー不足などにより実際的ではなく、現時点では一生涯にわたりインスリン注射が必要になる。 「今後、このCD8Tregの誘導メカニズムや膵臓での抑制メカニズムが明らかになることで、1型糖尿病の新たな予防・治療法の開発へつながると期待できます」と、研究者は述べている。 理化学研究所 生命医科学研究センター(IMS)CD8+ regulatory T cells play a critical role in prevention of autoimmune-mediated diabetes(Nature Communications 2020年4月22日)
[Terahata / 日本医療・健康情報研究所]