週1回投与デュアルGIP/GLP-1受容体作動薬「Tirzepatide」 2型糖尿病患者のHbA1cおよび体重を有意に減少
Tirzepatide最高用量群(15mg)で、HbA1cは2.07%低下し、体重は9.5kg(11.0%)減少した。この投与群の患者の半数以上(51.7%)は、HbA1cが5.7%未満に改善した。

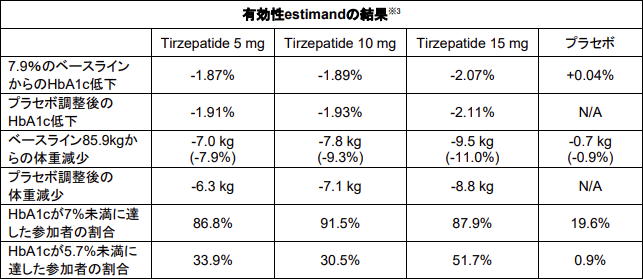
最高用量群(15 mg)の半数以上でHbA1cが正常範囲に改善
イーライリリー・アンド・カンパニーは、成人2型糖尿病患者を対象としたTirzepatide単剤療法の有効性と安全性を評価する臨床試験「SURPASS-1試験」で、ベースラインから40週投与後のHbA1c低下および体重減少を指標としたTirzepatideのプラセボに対する優越性が示されたと発表した。
Tirzepatideは、2型糖尿病治療のために開発されている新しいクラスの治療薬であり、グルコース依存性インスリン刺激性ポリペプチド(GIP)とグルカゴン様ペプチド(GLP-1)の両インクレチンの作用を単一分子に統合した新規の週1回投与デュアルGIP/GLP-1受容体作動薬だ。
一連のSURPASSプログラムの最初の第3相試験であるSURPASS-1試験は、食事と運動だけではコントロールが不十分な成人2型糖尿病患者を対象に、Tirzepatide 5mg、10mg、15mgの単剤療法の有効性と安全性をプラセボと比較した40週間の多施設共同無作為化二重盲検並行群間比較試験。同試験では、米国、メキシコ、インド、日本の478人の試験参加者を1:1:1:1:1の比率で無作為化し、Tirzepatide 5mg、10mg、15mg、またはプラセボのいずれかを投与した。
同試験の目的は、注射薬治療を過去に受けたことがなく、3ヵ月以内にいずれの経口血糖降下薬も使用していない2型糖尿病患者を対象に、40週後のベースラインからのHbA1cの低下をプラセボと比較し、Tirzepatide(5mg、10mg、15mg)の優越性を示すこと。この試験ではHbA1c 7%~9.5%、BMI 23以上の患者を組み入れた。全てのTirzepatide投与群の参加者は、週1回Tirzepatide 2.5mg投与の用量で試験を開始し、その後4週間間隔で段階的に増量し、最終の無作為化した維持用量である5mg(2.5mgの段階を経て)、10mg(2.5mg、5mg、7.5mgの段階を経て)、または15mg(2.5mg、5mg、7.5mg、10mg、12.5mgの段階を経て)を投与した。
試験参加者の54.2%は未治療で、糖尿病の平均罹病期間が比較的短い4.7年、ベースラインのHbA1cが7.9%、ベースラインの体重が85.9kgだった。
有効性estimand*を用いた評価から得られた結果は、Tirzepatide最高用量群(15mg)で、HbA1cが2.07%低下し、体重が9.5kg(11.0%)減少し、この投与群の患者の半数以上(51.7%)は、HbA1c 5.7%未満に改善したというものだった。
Tirzepatideの全体的な安全性プロファイルは、これまでに確立されたGLP-1受容体作動薬と同様であり、消化器系の副作用がもっとも多く報告された有害事象だった。有害事象による治療中止率は、Tirzepatideの各投与群で7%未満だった。
Dallas Diabetes Research Centerの部長でSURPASS-1試験の治験責任医師であるJulio Rosenstock氏は次のように述べている。 「Tirzepatideは、2018年に公表した第2相のデータにもとづき、そのデータを検証するために行った本試験で、優れた2型糖尿病患者のHbA1cおよび体重減少を示しました。本試験では通常よりも厳格なHbA1c目標達成率を評価しました。その結果、全参加者のほぼ90%がHbA1cのコントロール目標値である7%未満に達しただけでなく、最高用量群(15mg)の半数以上が糖尿病ではない人のレベルである5.7%未満のHbA1cに到達しました。これは血糖降下薬を評価する試験における前例のない知見でありユニークなエンドポイントでした」。
プラセボと比較した3種類のTirzepatideの用量(5mg、10mg、15mg)の群間差は、2つのestimand(有効性と治療方針)を用いて評価された。両estimandの評価を用いたTirzepatideの3用量全てで、ベースラインからのHbA1cと体重の減少、HbA1cが7%未満(米国糖尿病学会が糖尿病患者に推奨する目標)または5.7%未満に達した参加者の割合に統計学的有意差が認められた。
Tirzepatideの3用量全てで、ベースラインから統計学的に有意なHbA1cと体重の減少に加え、HbA1cが7%未満または5.7%未満に達した参加者の割合も統計学的有意差が認められた。
治療方針estimandで、Tirzepatideの各用量は統計学的に有意なHbA1cと体重の減少を示した。
■ HbA1c低下:-1.75%(5mg)、-1.71%(10mg)、-1.69%(15mg)、-0.09%(プラセボ)
■ 体重減少:-6.3kg(5mg)、-7.0kg(10mg)、-7.8kg(15mg)、-1.0kg(プラセボ)
■ HbA1cが7%未満 :81.8%(5mg)、84.5%(10mg)、78.3%(15mg)、23.0%(プラセボ)
■ HbA1cが5.7%未満 :30.9%(5mg)、26.8%(10mg)、38.4%(15mg)、1.4%(プラセボ)
Tirzepatide投与群に重症低血糖または54mg/dL未満の低血糖の発生は認められなかった。もっとも多く報告された有害事象は軽度から中等度の消化器関連であり、多くは投与量の増量期間中に認められた。同試験のTirzepatide投与群(それぞれ5mg、10mg、15mgの順)では、悪心(11.6%、13.2%、18.2%)、下痢(11.6%、14.0%、11.6%)、嘔吐(3.3%、2.5%、5.8%)、便秘(5.8%、5.0%、6.6%)の発生頻度がプラセボ(悪心6.1%、下痢7.8%、嘔吐1.7%、便秘0.9%)に比べて多く認められた。全体の治療中止率は、5mg群で9.1%、10mg群で9.9%、15mg群で21.5%、プラセボ群で14.8%だった。15mg群とプラセボ群の主な中止理由は、有害事象以外(コロナウイルスのパンデミックによる懸念、家族や仕事の都合など)によるものだった。
SURPASS-1試験の完全なデータはまだ評価されていないが、第81回米国糖尿病学会年次学術集会で公表され、2021年に論文化される予定。
週1回投与デュアルGIP/GLP-1受容体作動薬「Tirzepatide」
Tirzepatideは、グルコース依存性インスリン刺激性ポリペプチド(GIP)とグルカゴン様ペプチド(GLP-1)の両インクレチンの作用を単一分子に統合した週1回投与デュアルGIP/GLP-1受容体作動薬。GIPは、GLP-1受容体作動薬の効果を補完するホルモンだ。
前臨床モデルで、GIPは食物摂取量を減少させエネルギー消費を増加させることが示されており、体重の減少をもたらすと考えられる。また、GLP-1受容体作動薬と併用することでグルコースと体重に対してより大きな効果をもたらす可能性がある。
Tirzepatideは、成人2型糖尿病患者の血糖コントロールと慢性的体重コントロールのために第3相で開発中。また、非アルコール性脂肪肝炎(NASH)の治療薬としても研究されている。













